Фиксаторы
Джон Андерсон, Джонатан Ритл и Джонас Петерс из Калифорнийского технологического института предложили новые катализаторы фиксации азот. В природе фиксация атмосферного азота — важнейший процесс, который осуществляют почвенные микроорганизмы. Они переводят молекулярный азот в биологически доступную форму, и он включается в круговорот растительной биомассы. Многие годы исследователи пытаются найти химические катализаторы, которые хоть немного бы приближались по эффективности к природным.
Когда мы говорим «азот», не надо путать молекулу азота N2, которая существует в виде газа и составляет 78% объема атмосферы Земли, и атом азота, то есть химический элемент 15-й группы Периодической системы Д.И.Менделеева. Молекулярный азот N2 — это два атома азота, соединенные прочнейшей тройной ковалентной связью, разорвать которую очень непросто.
Открытием азота мы обязаны как минимум троим подданным британской короны — Джозеф Пристли, Генри Кавендиш и Даниель Резерфорд независимо друг от друга к 1772 году выделили его из атмосферного воздуха. Он был назван «мефитическим», или «испорченным воздухом» — это было связано с теорией флогистона, согласно которой в горючих веществах существует некая тонкая материя — флогистон, при сгорании уходящая в атмосферу. В отличие от кислорода — «горючего воздуха» — азот не поддерживал горения, за что его и признали «испорченным».
Название «азот» (греч. — безжизненный) больше подходит азоту-газу, а не элементу, поскольку без элементарного азота жизнь немыслима. Азот входит в состав большинства биологически активных молекул: аминокислот и белков, нуклеиновых кислот, гормонов, нейромедиаторов, витаминов и многих других. Откуда берут его животные и мы с вами? В основном из пищи, поедая других животных и растения, а растения, в свою очередь, усваивают азотистые соединения из почвы. Но химически стойкий молекулярный азот могут перерабатывать только некоторые почвенные микроорганизмы. Для того чтобы разорвать тройную связь, они используют несколько ферментов, важнейший из которых — нитрогеназа. «Перерабатывать» — не очень удачная формулировка, в научной литературе употребляют термин «фиксация азота». Именно ей посвящено исследование сотрудников Калтеха.
Фиксация — это, по сути, восстановление инертного азота до реакционноспособного аммиака. Как это делать в промышленных масштабах (с помощью температур, давления и катализаторов), более ста лет назад придумал Фриц Габер, за что получил Нобелевскую премию. А вот имитировать природный процесс, идущий благодаря нитрогеназе в обычных мягких условиях, пока не получается. Понятно, что для этого нужен хороший катализатор, который восстанавливал бы азот с высоким выходом. Но какой?
Нитрогеназа, как и многие другие ферменты, выполняет свою каталитическую функцию благодаря встроенному фрагменту небелковой природы. Именно он обеспечивает высокую специфичность биохимического превращения. В нитрогеназе эту роль играет железомолибденовый кофактор (FeMo-кофактор), то есть каталитический центр фермента содержит атомы железа и молибдена. И здесь возникает вопрос: к железу или к молибдену присоединяется молекулярный азот, чтобы потом приобрести лишние электроны? В более ранних работах были предложены два механизма процесса. Однако они подходят как для одного, так и для другого металла, отражая скорее предполагаемую механику фиксации.
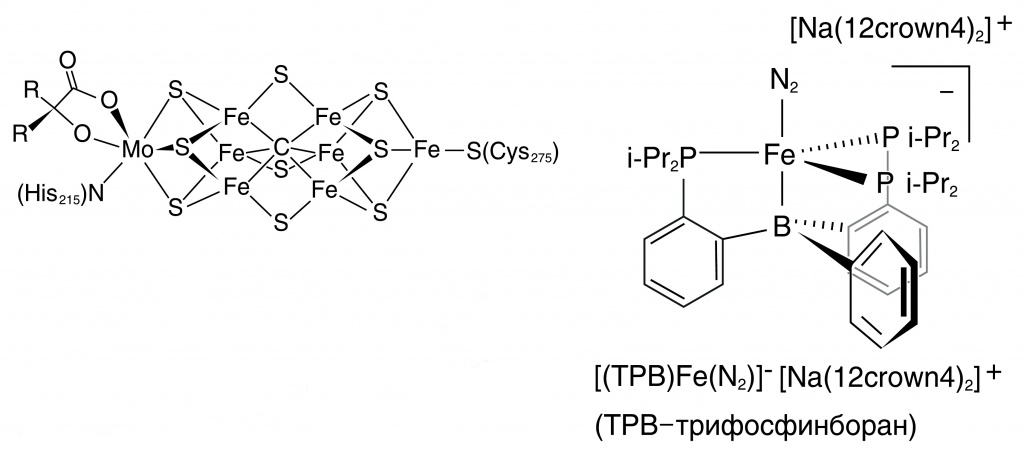
Довольно долго считалось, что главный в каталитическом центре нитрогеназы все-таки молибден. И действительно, химики за много лет исследований нашли некоторое количество молибденовых неорганических катализаторов, которые стехиометрически превращают в мягких условиях азот в аммиак. Но сейчас предполагают, что железо может выполнять фиксацию самостоятельно, без закадычного товарища. В частности, одним из аргументов служит то, что железо неизменно присутствует во всех нитрогеназах, а вот молибдена в этих ферментах может и не быть. Андерсон сосредоточил свои усилия на моделировании «железной» части кофактора. И ему удалось найти несколько вариантов комплексов железа и бора, лучшим из которых был [(TPB) Fe(N2)][Na(12crown4)2]. Если сравнивать с ранее описанными железными катализаторами, то новые соединения железа активнее во много сотен раз.
При этом, похоже, связь «железо-бор» оказалась уникальной. Другие варианты катализаторов без этой связки, например, когда бор заменили кремнием, работают гораздо хуже. Авторы исследования объясняют это тем, что связь Fe-B подвижна, поэтому фрагмент может присоединять не только аммиак, но и соединения NxHy, которые образуются во время реакции и, очевидно, играют важную роль в механизме фиксации. Калифорнийские ученые стремились доказать роль железной части FeMo-кофактора нитрогеназы. И им это удалось. Возможно, скоро химики перейдут от моделирования к более близким к практике исследованиям, и тогда крупнотоннажный процесс Габера-Боша наконец заменят на более безопасный и экологически чистый.
 |
|
В природном катализаторе фиксации азота (ферменте нитрогеназе) активый центр содержит железо и молибден. А синтетический комплекс для фиксации азота (справа) — железо и бор |
