Молекулярный металлодетектор
Химики из Департамента органической химии Индийской ассоциации развития науки во главе с доктором Джиотирмае Даш («Organic & Biomolecular Chemistry», 2013; doi: 10.1039/C3OB40075A) синтезировали сложное органическое соединение, которое назвали «кликафор». Оно работает как датчик на ионы цинка, кадмия и железа: образует с любым из этих ионов комплекс, который способен флуоресцировать: излучаемый им свет сигнализирует о наличии металла. Такой молекулярный приборчик может работать и в водном растворе при нейтральных значениях pH, и в живой клетке.
 |
|
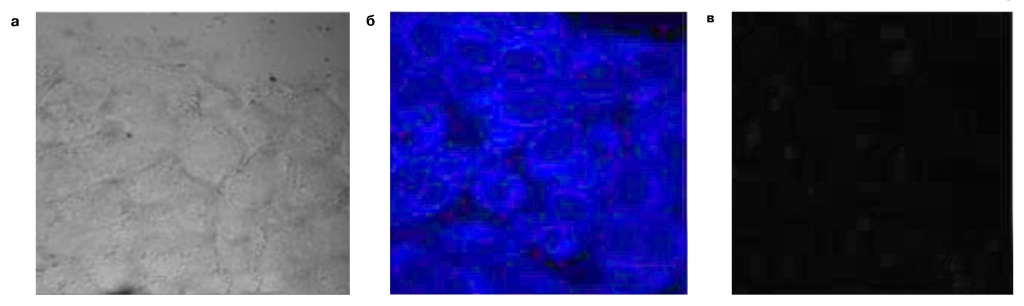
Культуру клеток (а) обработали сначала кликафором, а затем выдержали в растворе сульфата цинка и хлорида железа. После освещения ультрафиолетом клетки стали светиться. Экспериментальные, с цинком — ярко (б), а контрольные —в двадцать раз слабее (в), отчего фотография и представляет собой почти идеальный черный квадрат |
Интенсивность свечения комплексов кликафор-металл уменьшается в ряду: Zn2+>Cd2+>>Fe3+>>Cu2+>Fe2+. Исследователи приняли флуоресценцию комплекса с Fe2+ за точку отсчета и создали молекулярное логическое устройство для обнаружения цинка: если в растворе только ионы Fe2+ молекула засветится слабо, что будет ответом «нет». При наличии ионов цинка она даст сильную флуоресценцию — имеем ответ «да». Очевидно, метод можно использовать также для пары кадмий/трехвалентное железо.
В работе индийских ученых отразились характерные тенденции современной химии. Это не только использование флуоресцентных свойств молекулы и концепция молекулярных логических устройств, но и методы так называемой клик-химии (отсюда и название вещества: «клик» + «флуорофор»). Клик-химия — развивающееся в последнее десятилетие направление органического синтеза, в котором большие молекулярные структуры создают из малых молекул (в подражание природе); реакции при этом должны проходить быстро, с минимумом побочных продуктов и без применения высокого давления или температуры. Последнее важно для работы подобных соединений в живых системах.
Биологическая активность переходных металлов — причина, по которой нужно контролировать их содержание в воде и продуктах питания. Например, цинк — жизненно необходимый микроэлемент: выступает в роли кофактора во многих ферментах, необходим для синтеза белков и нуклеиновых кислот. Однако кадмий, сосед цинка по подгруппе IIБ, очень ядовит: он замещает цинк и выводит из строя содержащие этот металл ферменты. В результате снижается иммунитет, и дело может закончиться злокачественным новообразованием. Кликафор же способен отлавливать ионы металлов не только в растворе, но ив живой клетке и, светясь в ней, сообщать о присутствии ядовитого элемента.
Благодаря своим замечательным свойствам кликафор наверняка найдет применение и как лабораторный реагент, и как сенсорный материал для приборов-индикаторов.
 |
|
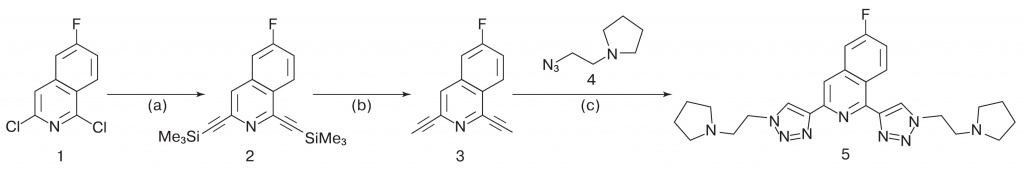
Циклические части молекулы кликафора получают с помощью азидов — соединений, содержащих группу —N3. Эта характерная для клик-химии реакция протекает при комнатной температуре, давая лишь 1% побочных продуктов |
