
Подписаться
Подписаться
Закат «цинкового мира», прокариотная биосфера и происхождение фотосинтеза

Теория «цинкового мира», среди прочего, легко и естественно объясняет расхождение линий бактерий и архей и появление их отличительных свойств. Ранее для их разделения предлагали географическую изоляцию, но сама по себе изоляция не создала бы таких фундаментальных различий. В «цинковом мире» их пути расходятся, когда падение давления атмосферы более не позволяет геотермальным источникам выносить на поверхность сульфид цинка. Его старые отложения тают под солнечным светом, расходуясь на абиогенный фотосинтез, который мы обсуждали в апрельском номере, и населяющие их протоорганизмы оказываются в кризисе. Из этого кризиса они нашли два выхода. Одна группа, давшая начало бактериям, покинула геотермальные биотопы и научилась использовать энергию света самостоятельно, с помощью пигментов, из которых впоследствии сохранился хлорофилл. Они, скорее всего, произошли от обитателей верхних, самых освещенных слоев отложений ZnS, где еще до кризиса им пришлось создать пигментные системы для защиты от ультрафиолета мембран и мембранных белков. Другая группа не смогла отказаться от родной геотермальной химии и последовала за тающими сульфидными источниками в морские глубины и вечную темноту. Им пришлось освоить хемоавтотрофное питание, например используя энергию реакции метаногенеза: CO2 + 4H2 → CH4 + 2H2O. Они стали археями.
Обе группы изгнанников из «цинкового рая» столкнулись с похожими проблемами, первая из которых — дефицит цинка и обилие ионов железа, натрия и кальция. Им пришлось сделать мембраны непроницаемыми для ионов металлов, чтобы сохранить привычную химическую обстановку хотя бы в своей цитоплазме. Для этого были созданы двухвостые липиды с глицерином. Им также понадобились системы транспорта, переносящие цинк и другие ценные металлы, такие, как марганец, внутрь клетки и откачивающие опасные железо, кальций и натрий наружу. Железо, как мы уже говорили, легко гидролизует РНК, кальций же замещает магний в его комплексах с нуклеотидами и РНК, останавливая разные ферментативные реакции с их участием. Натрий не так опасен, но и его концентрация на уровне морской воды нарушает структуру ДНК и белков. Для защиты от железа пришлось перейти от гетеродуплексного ДНК-РНК-генома к двухцепочечной ДНК, после чего многоплазмидный геном путем рекомбинаций собрался в одну кольцевую молекулу ДНК. Это позволило миниатюризировать клетки, они стали маленькими по сравнению с плоскими, сидящими на минералах протоорганизмами.
Различие в составе липидов бактерий и архей (см. статью в предыдущем номере) отражает разные исходные условия их жизни. Бактерии сменили терпеноспирты на жирные кислоты, так как двойные связи в молекулах терпенов уязвимы к ультрафиолетовому излучению Солнца. Липиды с двойными связями, в свою очередь, сохраняют структуру мембраны в широком диапазоне температур, что важно для обитателей «черных курильщиков». Выходы горячей воды в них могут неожиданно исчезать и появляться, поэтому их обитатели должны быть готовы в любой момент попасть из кипятка в холодную воду и обратно.
Существует и другая теория относительно происхождения архей. Ее выдвинул британский биолог Томас Кавалье-Смит, автор множества радикальных идей. По Кавалье-Смиту, археи произошли от бактерий достаточно поздно в истории Земли — около 1 миллиарда лет назад, после 2,5 миллиарда лет существования чисто бактериальной биосферы, а все глубокие отличия архей от бактерий появились как приспособления к жизни при высоких температурах (Cavalier-Smith, «International Journal of Systematic and Evolutionary Microbiology», 2002, 52, 1, 297—354, doi: 10.1099/ijs.0.02058-0). Согласно этой теории, называемой обычно теорией Neomura, молекулярно-филогенетические деревья, помещающие общего предка всех клеток между бактериями и археями, искажены из-за ускоренной эволюции в основании архейной ветви, а если ввести на это поправку, то общий предок оказывается среди разных ветвей бактерий. Название «Neomura» (буквально «новые стенки») относится к группе, объединяющей архей и эукариот, и отражает их серьезные отличия в составе и путях построения клеточных стенок и механизмах секреции белков из клетки. По мнению Кавалье-Смита, чтобы приспособиться к высоким температурам, археям пришлось изменить путь секреции белков и усилить контроль точности их синтеза, а это повлекло за собой каскад из десятков перестроек в разных клеточных системах, включая рибосомы и репликативную вилку. Дальше предок архей освоил сверхгорячие экологические ниши, для чего потребовалось изменить и состав мембранных липидов, а предок эукариот остался с липидами бактериального типа.
Некоторые ученые поддерживают эту теорию, но она далека от общепринятой. Современные филогенетические методы позволяют обнаружить большинство искажений филогенетических деревьев из-за временного ускорения эволюции в отдельных группах, хотя и не могут их устранить. Но в случае архей такое ускорение эволюции по сравнению с бактериями не выявляется. И главное — как мы помним, в мембранах бактерий и архей используются разные стереоизомеры глицеринфосфата, идентичные по всем физико-химическим свойствам. Никакой естественный отбор не способен вызвать замену одного изомера на другой. Мембраны бактерий и архей могли произойти либо от предковой мембраны с однохвостыми липидами без глицерина, либо от смешанной мембраны с двумя изомерами глицеринфосфата, хотя жизнеспособность этого варианта вызывает серьезные сомнения. Так что основные утверждения теории Neomura, скорее всего, будут отвергнуты по мере накопления новых данных.
Итак, сколько-то миллионов лет после расхождения линий бактерии и археи оставались в изоляции. Иногда только бактерий сносило с мелководий в открытое море, они тонули, и их ДНК попадала в сообщества архей. Поэтому событий горизонтального переноса генов от бактерий к археям известно намного больше, чем в обратную сторону. Затем бактерии образовали жгутики, освоили плавание и смогли заселить открытое море. Археи, в свою очередь, совершенствовали защитные системы, наращивали разнообразие метаболизмов и со временем смогли выйти из «черных курильщиков» в другие местообитания. Так живые археи вошли в контакт с живыми бактериями и образовали единое сообщество.
Возникла достаточно разнообразная прокариотная биосфера, заселившая практически всю поверхность Земли и дно океанов. Основными продуцентами в ней были бактерии, осуществлявшие сульфидный фотосинтез:
CO2 + 2H2S → C6H12O6 + H2O +2S.
В этом процессе сероводород окисляется до молекулярной серы, а с дополнительными ферментами и до тиосульфата, сульфита и сульфата (SO4 2-).
Создаваемую ими органику потребляли разнообразные гетеротрофы (так называются организмы, не способные синтезировать органику из неорганики, в отличие от автотрофов — фотосинтетиков и хемосинтетиков). Одни использовали сульфатное дыхание — реакцию, обратную сульфидному фотосинтезу. В ней сульфат восстанавливается до сероводорода, а органика — до CO2 и воды. Окисление глюкозы сульфатом дает до 14 молекул АТФ на одну молекулу глюкозы, что значительно продуктивнее гликолиза, хотя и не дотягивает до эффективности кислородного дыхания (38 молекул АТФ на одну глюкозы).
Другие гетеротрофы освоили разнообразные реакции брожения. Среди них были молочнокислые бродильщики, маслянокислые, пропионовокислые, уксуснокислые и другие. Особо надо отметить уксуснокислых бродильщиков, или ацетогенов: в их метаболизме, наряду с ацетатом, из сахаров образуются CO2 и водород, поэтому метаногенные археи, вошедшие в состав бактериальных сообществ поверхности Земли, всегда живут вместе с ацетогенами: восстанавливая углекислый газ водородом, они как раз и производят метан.
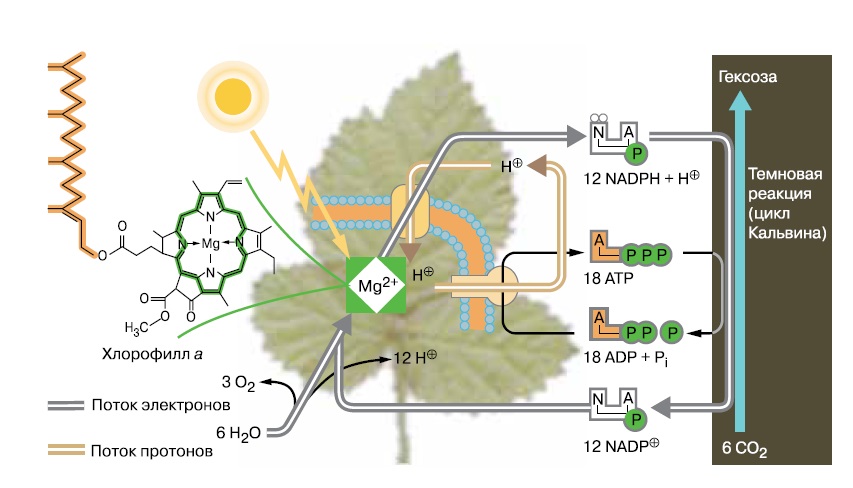
О происхождении фотосинтеза могут рассказать последовательности участвующих в нем белков и пути биосинтеза пигментов. Процесс фотосинтеза, как он описан в школьных учебниках, состоит из световых и темновых реакций (рис. 1). Световые реакции сводятся к синтезу АТФ и восстановителей, таких, как НАДФН, при помощи света и какого-либо донора электронов. Темновые реакции — это восстановление CO2 при помощи НАДФН и АТР в цикле Кальвина или, реже, в обратном цикле Кребса, они уже обсуждались в апрельском номере.
|
| 1. Обобщенная схема фотосинтеза. Энергия фотонов необходима, чтобы получать из воды кислород, электроны и протоны, за счет протонного градиента синтезировать АТФ, а также восстановитель НАДФН. Молекулы АТФ и НАДФН расходуются на синтез шестиатомных углеводов из СО2 в цикле Кальвина — эти реакции могут протекать и в темноте (по: Ян Кольман, Клаус-Генрих Рем, Юрген Вирт, «Наглядная биохимия») |
Темновые реакции не уникальны для фотосинтеза. Тот же цикл Кальвина работает и при хемосинтезе, и его ферменты, скорее всего, исходно работали в связке с кристаллами сульфида цинка в качестве восстановителя.
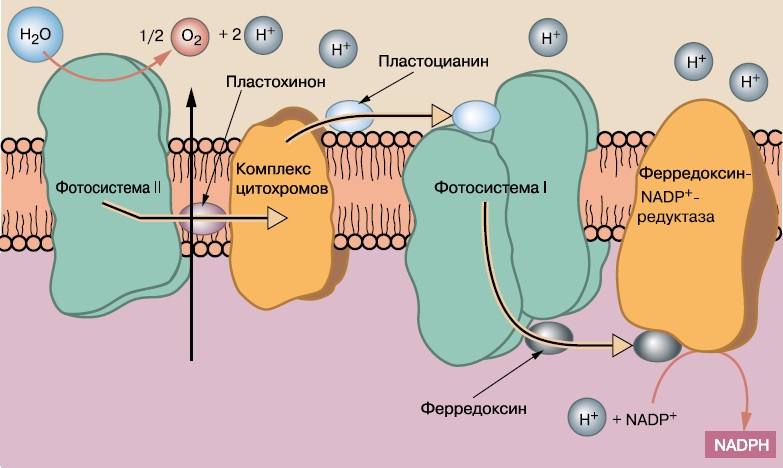
Напомним структуру фотосинтетического аппарата зеленых растений. Его функциональное ядро составляют реакционные центры — встроенные в мембрану белковые молекулы из нескольких похожих доменов, с которыми связаны молекулы хлорофилла, по две в каждом реакционном центре. Возбужденные молекулы хлорофилла передают электроны на акцепторы. Реакционные центры делятся на два класса: фотосистемы I типа (ФСI) переносят электроны на ферредоксин — водорастворимый белок с железо-серным кластером, а фотосистемы II типа (ФСII) — на хиноны, плавающие в мембране (рис. 2).
|
| 2. Схема переноса электронов при фотосинтезе |
В клетках цианобактерий и в хлоропластах растений присутствуют оба типа фотосистем одновременно, а фотосинтезирующие бактерии обладают только одним типом. Электроны ФСI через ферредоксин переносятся на НАДФ и далее используются в реакциях восстановления разных органических веществ. Электроны ФСII попадают в электрон-транспортную цепь, где их энергия тратится на транспорт протонов через мембрану и в конечном счете — на синтез АТФ. В цианобактериях и хлоропластах растений окисленная ФСII с помощью водоокисляющего комплекса восполняет недостающие электроны из молекул воды, окисляя их до кислорода, а ФСI принимает электроны, прошедшие электрон-транспортную цепь и ФСII. Хиноны, ферредоксин, а также пластоцианин транспортируют электроны от ФСII к цитохромам, от цитохромного комплекса к ФСI и от нее к ферменту, синтезирующему НАДФН. Кроме того, возможен циклический транспорт электронов по маршруту ФСII — электрон-транспортная цепь — ФСII. Реакционные центры окружены большим количеством антенных белков, также связывающих хлорофилл, — эти белки поглощают световые кванты и передают возбуждение на реакционные центры.
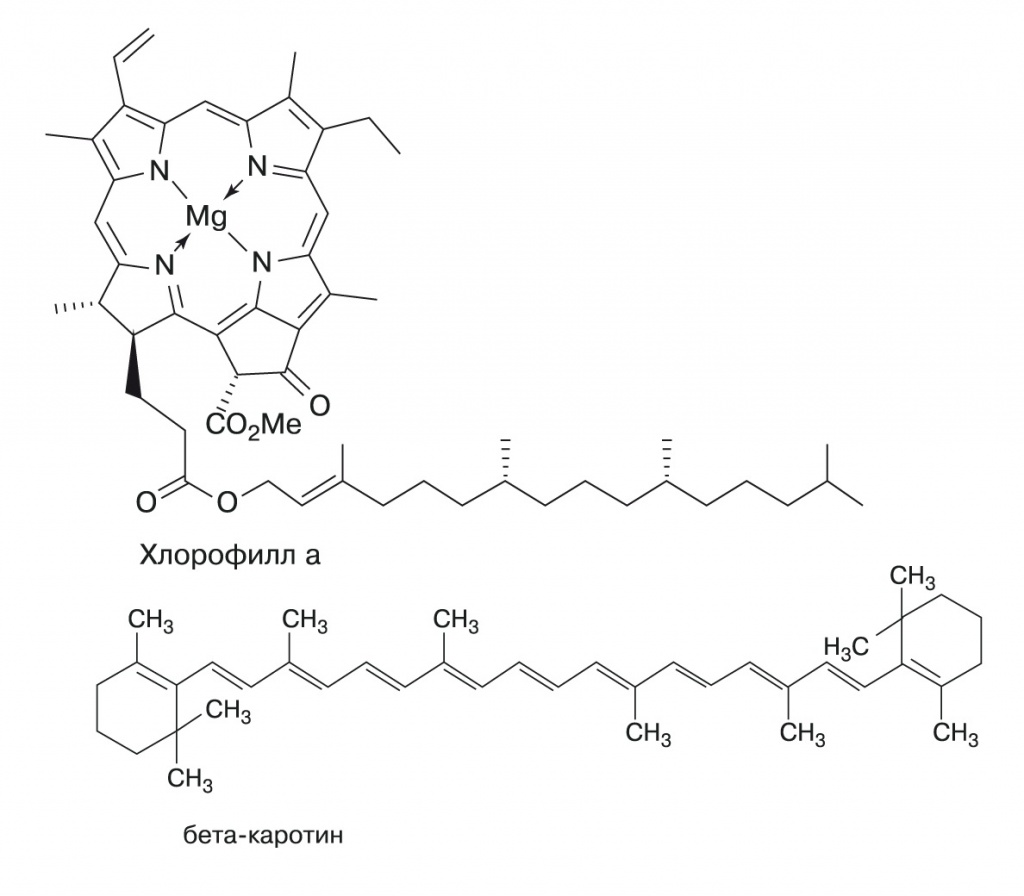
Кроме хлорофиллов в фотосинтезе участвуют пигменты каротиноиды. Они поглощают свет в голубом и зелено- голубом участках спектра и передают возбуждение на хлорофилл (рис. 3).
|
| 3. Фотосинтетические пигменты |
Как же образовалась столь сложная система пигментов и электрон-транспортных цепей? В апрельском номере мы рассказывали, что в состав живых систем с самого начала входили молекулы с особыми фотохимическими свойствами. Например, все азотистые основания эффективно рассеивают энергию ультрафиолетового света в тепло, защищая соседние молекулы.
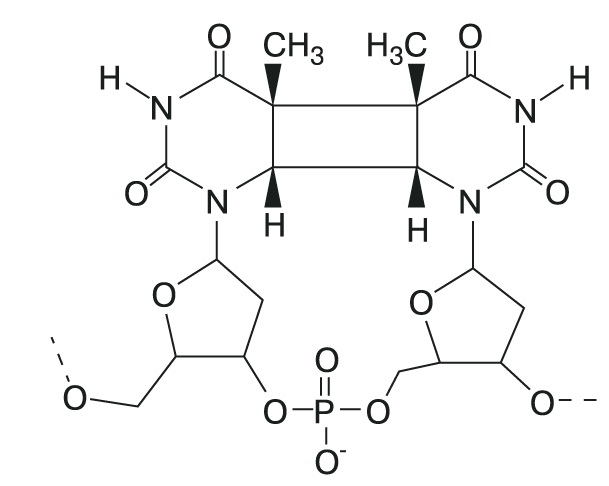
Адениновые нуклеотиды в растворе также способны за счет энергии света присоединять фосфатные группы, синтезируя АТФ. Древние окислительно-восстановительные коферменты, такие, как НАД и ФАД, тоже могли пройти отбор на особые фотохимические свойства. Для ФАД известна одна реакция, требующая энергии света. Это реакция восстановления тиминовых димеров — одного из продуктов повреждения ДНК ультрафиолетом (рис. 4).
|
| 4. Тиминовый димер в ДНК |
Тиминовый димер содержит четырехчленный цикл, который узнает ФАД-содержащий фермент фотолиаза. Для разрушения одинарных С—С связей четырехчленного цикла нужна большая энергия, и ее поставляет квант синего света, который поглощает восстановленная форма ФАД. В темноте фотолиаза не работает. Возможно, реакции такого типа были первой функцией ФАД и НАД на заре РНК-мира.
У животных и растений на основе бактериальной фотолиазы возникли криптохромы — ФАД-содержащие светочувствительные белки, регулирующие суточные и сезонные ритмы. Как ни удивительно, у животных криптохромы также участвуют в восприятии магнитного поля — при помощи магниточувствительной реакции с анион-радикалом кислорода («Biophysical Journal», 2009, 96, 12, doi: 10.1016/j. bpj.2009.03.048).
Другая группа светопоглощающих пигментов живых клеток — каротиноиды — тоже имеет разнообразные интересные функции. Один из каротиноидов, ретиналь, поглощает синий и голубой свет и превращает их энергию в механические изгибы — меняет форму с прямой на изогнутую и обратно. В комплексе с мембранными белками бактериородопсинами ретиналь может переносить протоны, ионы натрия и даже ионы хлора через мембрану. Пропуская эти ионы обратно через вращающуюся мембранную АТФазу, клетка получает АТФ за счет энергии света при помощи лишь одного дополнительного белка. Такая система гораздо надежнее и устойчивее к экстремальным условиям, чем сложные хлорофиллсодержащие фотосистемы. Бактериородопсины были впервые найдены у Halobacterium halobium, населяющей пересоленные лагуны, но в последнее время обнаружено, что они широко распространены у самых разных морских и пресноводных бактерий и позволяют им подолгу активно плавать без пищи. Родственные ретинальсодержащие белки — родопсины — работают в органах зрения всех животных, и благодаря им вы можете читать этот текст. В глазах у одной глубоководной рыбы обнаружен хлорофилл, позволяющий ей видеть в ближнем инфракрасном диапазоне! («Nature», 1998, 393(6684), doi: 10.1038/30871.)
Каротиноиды относятся к терпеновым веществам, гидрофобны и часто находятся в мембранах среди липидов. Самые распространенные С30-каротиноиды, такие, как бета-каротин, лежат в мембране параллельно хвостам липидов, проходя от одной стороны мембраны до другой. Скорее всего, изначально, на самых ранних этапах эволюции мембран, они защищали двойные связи древних липидов от повреждения ультрафиолетом, снимая с них возбуждение и рассеивая его в тепло.
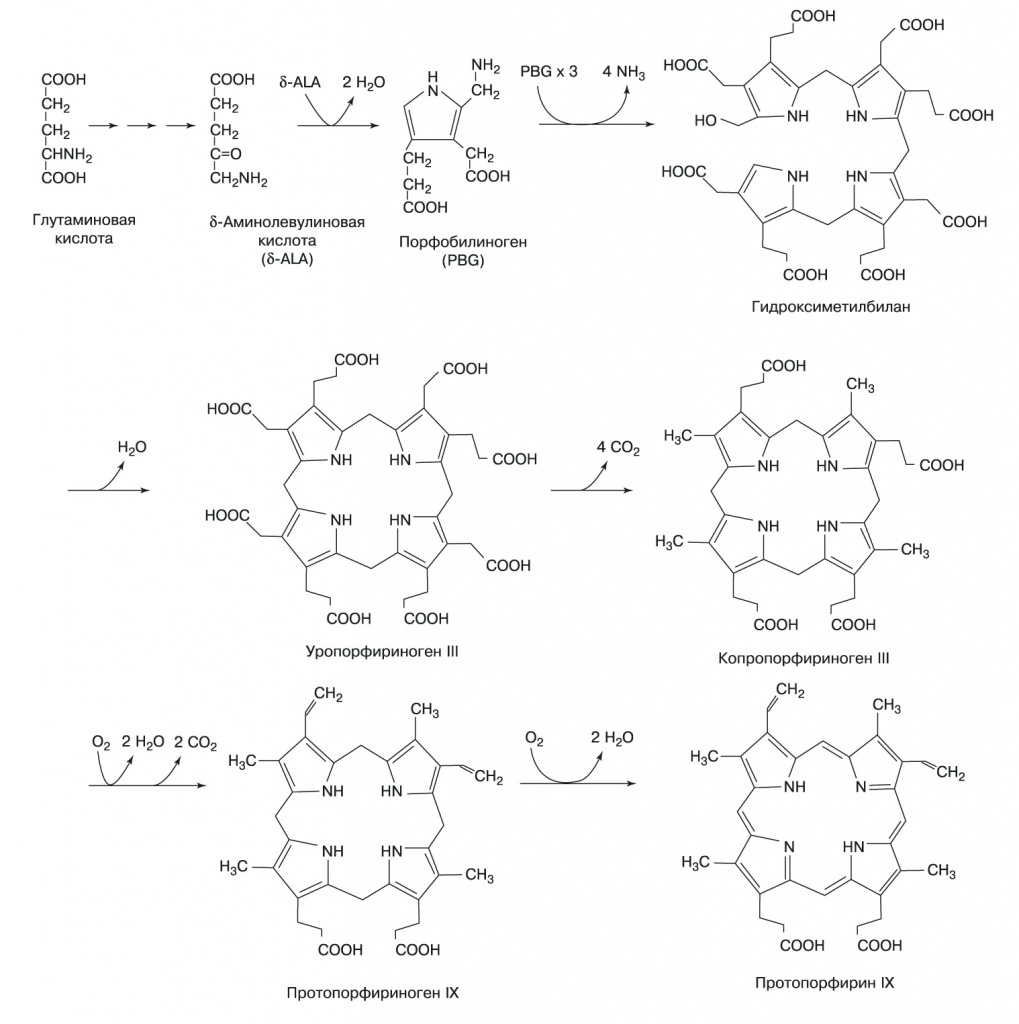
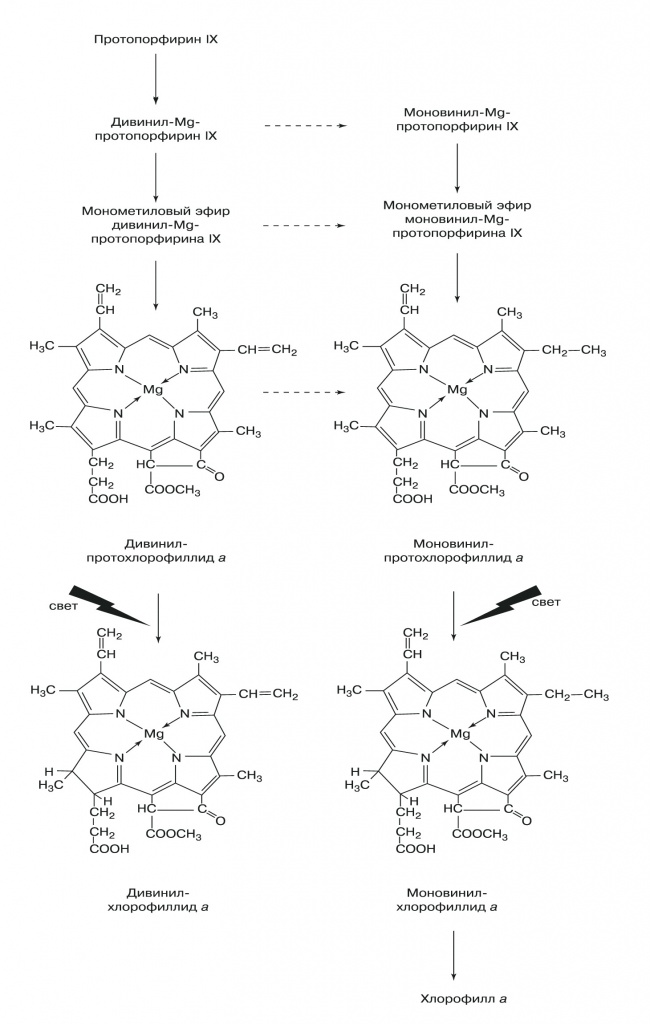
Реакционные центры фотосинтетического аппарата содержат два типа пигментов: хлорофилл a (цианобактерии и хлоропласты) и бактериохлорофилл a (фотосинтезирующие бактерии, кроме цианобактерий). Синтез всех пигментов начинается с глутаминовой кислоты, которая в несколько стадий превращается в дельта-аминолевулиновую кислоту. Ее молекулы объединяются попарно в циклическое соединение — порфобилиноген. Из четырех молекул порфобилиногена собирается тетрапиррольное кольцо гемов и хлорофиллов — до стадии протопорфирина IX их пути синтеза совпадают. Потом к молекуле протопорфирина IX присоединяется атом магния, и через еще несколько промежуточных продуктов образуется хлорофилл (рис. 5, 6).
|
| 5. Общая часть путей биосинтеза хлорофиллов и гемов |
|
| 6. Синтез хлорофилла а из протопорфиринов |
Зеленый цвет хлорофилла обусловлен тем, что он поглощает свет в двух диапазонах — красном и сине-фиолетовом. Причем в обоих вариантах молекула попадает в одно и то же возбужденное состояние: избыточная энергия синего кванта рассеивается в тепло. Если исследовать хлорофилл, экстрагированный из листьев, например, спиртом, у него можно заметить красную флюоресценцию при облучении синим или фиолетовым светом. У предшественников хлорофилла — хлорофиллидов, протохлорофиллидов, протопорфирина IX, уропорфирина и уропорфириногена — эта флюоресценция выражена сильнее, а полоса поглощения сдвинута в ближнюю ультрафиолетовую область.
Хлорофилл-связывающие белки обоих типов реакционных центров, так же как главные антенные белки CP43 и CP47 цианобактерий и хлоропластов и светособирающие комплексы зеленых несерных бактерий (LH), состоят из похожих трансмембранных доменов; к некоторым доменам прикрепляются молекулы хлорофилла. Возбуждение на хлорофилл передается через остатки ароматических аминокислот — тирозина, триптофана, гистидина, — которые близко прилежат к нему.
Выравнивание последовательностей этих белков друг с другом показывает, что все они могли произойти от одного предкового мембранного белка, имевшего 11 одинаковых доменов, с молекулами хлорофилла либо его предшественников на каждом домене («Journal of Molecular Evolution», 2005, 60, 2, 153, doi: 10.1007/s00239-003-0181-2; «Photosynthesis Research», 1997, 51, 1, 27, doi: 10.1023/A:1005726809084). Исходной его функцией, как и у каротиноидов, могла быть защита от ультрафиолета: возможно, такой белок эффективно снимал возбуждение с соседних молекул и рассеивал его частью в тепло, частью в красную флюоресценцию.
Такая защита могла быть востребована еще на стадии РНК-белкового мира: протоорганизмы того времени уже имели мембраны, удаленные от минеральной подложки и не защищенные от УФ сульфидом цинка. Плавающие расселительные стадии выигрывали от наличия такого белка еще больше. В современных реакционных центрах появились сайты связывания акцепторов электронов (хинонов и ферредоксина), а некоторые домены утратили способность к связыванию хлорофилла, причем в ФСI и ФСII это были разные домены. Расположение вспомогательных молекул хлорофилла и феофитина, необходимых для эффективного однонаправленного электронного переноса внутри фотосистемы, сильно отличается в ФСI и ФСII, и, скорее всего, они независимо произошли от древнего УФ-защитного белка.
Современные бактерии, обладающие ФСI, как правило, используют сероводород и другие восстановленные формы серы в качестве доноров электронов. Они фиксируют CO2 и восстанавливают его электронами, проходящими через ФСI и ферредоксин. Обладатели ФСII имеют менее обычный фотосинтез. Одни, например зеленые нитчатые несерные бактерии, вообще не фиксируют CO2, свет им нужен только для получения АТФ благодаря циклическому транспорту электронов. Внешние доноры электронов им не требуются. Другие, например пурпурные бактерии, фиксируют CO2 и могут использовать в качестве доноров электронов как соединения серы, так и более слабые восстановители — ионы двухвалентного железа и марганца. ФСII имеет более низкий редокс-потенциал, чем ФСI, как в окисленной, так и в восстановленной форме. Поэтому она может брать электроны от более слабых восстановителей, но не может прямо передавать их на ферредоксин. Пурпурные бактерии используют обратный транспорт электронов для восстановления ферредоксина: часть электронов движется против редокс-градиента за счет протонного мембранного потенциала, что требует достаточно сложной электрон-транспортной цепи.
В условиях исчерпания сероводорода в окрестностях бактериальных сообществ способность ФСII использовать другие доноры электронов, прежде всего двухвалентное железо, обильное в водах древнего океана, стала серьезным конкурентным преимуществом. В наиболее выигрышном положении оказался предок цианобактерий, совместивший в себе путем горизонтального переноса ФСI и ФСII, — он мог использовать железо и марганец гораздо эффективнее, не прибегая к обратному транспорту электронов. На этой стадии эволюции было отработано сопряжение двух фотосистем, а также циклического и нециклического транспорта электронов.
Системы защиты от токсического действия кислорода, необходимые для кислородного фотосинтеза, скорее всего, возникли тогда же. Показано, что на поверхности пирита FeS2 при освещении в воде образуется перекись водорода Н2О2. Ионы Fe3+ — продукт железозависимого фотосинтеза — тоже образуют перекись водорода при освещении раствора, так что каталаза и другие защитные системы могли возникнуть вскоре после выхода бактерий из «цинкового мира». Более того, водоокисляющий комплекс современных цианобактерий может использовать Н2О2 в качестве донора электронов, причем для этого требуется меньше энергии света, чем для окисления воды. Возможно, утилизация перекиси водорода в фотосинтезе была первой функцией примитивного водоокисляющего комплекса. Существуют противоречивые данные о роли Н2О2 в современном кислородном фотосинтезе — в зависимости от изучаемого вида и условий, перекись может как подавлять его, так и стимулировать. Некоторым видам цианобактерий для выделения кислорода необходимо, чтобы заметное количество кислорода уже содержалось в среде. Как это объяснить — пока непонятно («Photosynthesis Research», 2004, 80, 373, doi: 10.1023/B:P RES.0000030457.06495.83).
Окисление воды — сложная задача. Редокс-потенциал бактериохлорофилла а (0,55 V) достаточен для окисления H2S и других серосодержащих соединений. Редокс-потенциал хлорофилла а из цианобактерий выше, около 0,82 V. Однако если окислять воду в одноэлектронных процессах, то первая реакция, превращающая воду в гидроксильный радикал и протон, требует огромного редокс-потенциала — 2,75 V, недоступного ни для каких фотосинтетических пигментов. Поэтому необходим промежуточный переносчик электронов, способный окислить сразу две молекулы воды, — редокс-потенциал хлорофилла будет достаточен, только если его равномерно делить на четыре электрона.
Водоокисляющий комплекс — белок, содержащий четыре иона марганца, которые меняют степень окисления от +3 до +4. Ионы марганца составляют марганец-кислородный кластер, кроме того, с ним связано по одному иону кальция и хлора. Структура этого кластера напоминает элементарную ячейку таких природных минералов, как ранциеит (CaMn4O9 ∙ 3H2O) и других слоистых оксидов марганца, — аналогичным образом FeS-кластеры окислительно-восстановительных ферментов, о которых мы рассказывали в июньском номере, похожи на ячейку пирита. Существовала гипотеза о происхождении комплекса от защитного фермента супероксиддисмутазы, одна из разновидностей которого содержит два иона марганца. Такой примитивный фермент мог быть способен к двухэлектронным реакциям — окислению Н2О2 до кислорода.
Окисление воды до Н2О2 в такой системе было невозможно из-за недостаточного редокс-потенциала хлорофилла. Однако никакого сходства между последовательностями супероксиддисмутаз и белков водоокисляющего комплекса обнаружено не было, кроме того, вряд ли в архейских морях было достаточно перекиси водорода, чтобы она заслуживала внимания как донор электронов.
Было замечено, что выделение кислорода в фотосинтезе сильно стимулируется добавлением бикарбонатов, солей HCO3- . Изотопное мечение показало, что бикарбонат-ион прямо конкурирует с кислородом за активный центр водоокисляющего комплекса. Кроме того, бикарбонат необходим для сборки марганцевого кластера: в воде хорошо растворим только Mn 2+, и в процессе сборки эти ионы под действием света окисляются до Mn 3+. В эксперименте после отделения марганцевого кластера от водоокисляющего комплекса ФС II достаточно добавить Mn(HCO3) 2 при освещении, чтобы марганцевый кластер постепенно собрался заново. В присутствии бикарбоната в водном растворе образуются марганец-бикарбонатные кластеры без всяких белков, кроме того, по редокс-потенциалу такие кластеры могут служить донорами электронов для бактериальных фотосистем.
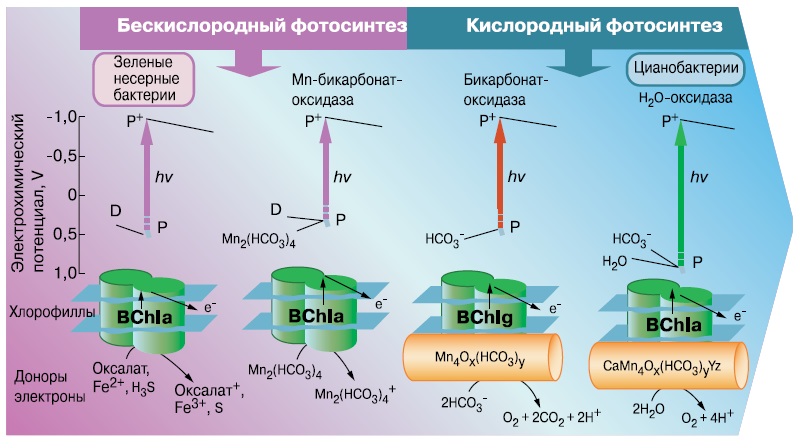
Наиболее вероятный сценарий происхождения кислородного фотосинтеза на основе этих фактов опубликовала группа биофизиков из Института фундаментальных проблем биологии в Пущино и Принстонского университета (Dismukes и др., «Proceedings of the National Academy of Sciences», 2001, 98, 5, 2170—2175, doi: 10.1073/pnas.061514798). Сначала бикарбонаты марганца заменили сероводород и железо в роли донора электронов (рис. 7). Затем на ФСII собрался марганец-бикарбонатный кластер, способный катализировать фотоокисление HCO3- до кислорода и CO2, — эта реакция требует в полтора раза меньше энергии, чем окисление воды, и возможностей бактериальной ФСII для этого практически достаточно.
|
| 7. Происхождение кислородного фотосинтеза (Dismukes et al., 2001). Буквой P обозначены электрохимические потенциалы реакционных центров хлорофилла на каждом этапе эволюции, D — конечных доноров электронов (формиата, оксалата) |
Далее бактериохлорофилл a в составе ФСII был заменен более редокс-активным пигментом, таким, как бактериохлорофилл g, для повышения скорости этой реакции. Наконец, по мере истощения запасов CO2 в атмосфере и бикарбонатов в море к марганцевому кластеру присоединился ион кальция, повысивший его редокс-потенциал и сделавший возможным окисление воды, и хлорофилл а, ускоривший реакцию благодаря дополнительному повышению редокс-потенциала. А это уже практически современный фотосинтез.
Элементы жизни: почему не кремний и не фтор
Фотохимия и «черные курильщики»
Пути восстановления углекислого газа
Происхождение белкового синтеза и генетического кода
Мир вирусов, последний общий предок и происхождение ДНК
Происхождение мембран и мембранной биоэнергетики
Закат «цинкового мира», прокариотная биосфера и происхождение фотосинтеза