Водородные картриджи
Что еще может быть источником водорода, например на борту автомобиля?
Известно, что водород хорошо растворим во многих металлах, например в некоторых щелочноземельных и металлах платиновой группы. В лабораторной технике уже применяются источники водорода, работающие на этом принципе. Скажем, в баллоне, заполненном магнием, можно растворить водород, а потом потихоньку высвобождать его — для этого достаточно просто подогреть баллон. Выделяющийся водород очень чистый (99,999%) и пригоден даже для атомного реактора. Однако у этого метода есть и существенные недостатки: огромная масса такого источника водорода, невысокая скорость высвобождения и сложность управления этим процессом.
Отдельное направление в мировых исследованиях занимают вещества на основе боранов и борогидридов щелочных металлов. Американская компания «Millennium-Cell» предлагает использовать в качестве источника водорода 5%-ный щелочной раствор борогидрида натрия:
NaBH4 + 2H2O → 4H2 + NaBO2
Если в раствор опустить рутениевый катализатор, то из него с хорошей скоростью начинает выделяться водород. Такой реакцией управлять довольно просто, а почистить выделяющийся водород можно, скажем, пропустив его через палладиевую мембрану.
Но одна из основных целей водородной энергетики — это экологическая безопасность и возобновляемость исходных веществ, иначе она теряет свой первоначальный смысл. Образующийся же в этой реакции метаборат натрия неудобно регенерировать в исходный борогидрид в промышленных масштабах, поскольку это требует высоких температур и реакция проходит с малым выходом.
Водород из борогидрида натрия также выделяется при реакции со спиртами в органических растворах. Огромное преимущество — образующиеся продукты (эфиры бора и алкоголяты натрия) легко регенеруются, превращаясь в исходный борогидрид:
Реакция:
L·NaBH4 + 4ROH → 2H2 + B(OR)3 + NaOR + L ,
где L — макроциклический лиганд,
ROH — первичный спирт.
Регенерация:
B(OR)3 + 4NaH → NaBH4 + 3NaOR,
3NaOR + 2B2H6 → 3NaBH4 + B(OR)3,
NaBH4 + L → L·NaBH4
Но и в этом методе есть проблемы. Борогидриды щелочных металлов плохо растворяются в органических растворителях, а водород выделяется с небольшой скоростью.
В этом направлении дальше других продвинулись ученые Института физической химии РАН. Они связали борогидрид натрия с различными бензозамещенными краун-эфирами. Натрий оказался в полости макроцикла,связанный атомами кислорода или азота, а противоионом стал борогидридный анион. Связанные борогидриды не только существенно лучше растворяются в органических растворителях, но и реакция выделения водорода с ними становится управляемой — ее скорость можно менять, например, скоростью подачи реактива. Водород получается очень чистым и по качеству не уступает тому, который получен другими методами производства особо чистого водорода. Продукты реакции регенерируемы, а значит, процесс экологичен.
Возможно, такие способы в недалеком будущем принципиально изменят всю схему заправки нестационарных объектов. Топливо не будут необратимо сжигать, а станут использовать картриджи. Такой картридж ставится на борт автомобиля или другого объекта, водород, извлекаемый из картриджа, дает энергию двигателю (см. схему), а после полного расходования картридж возвращается на дозаправку, где производится регенерация исходных веществ.
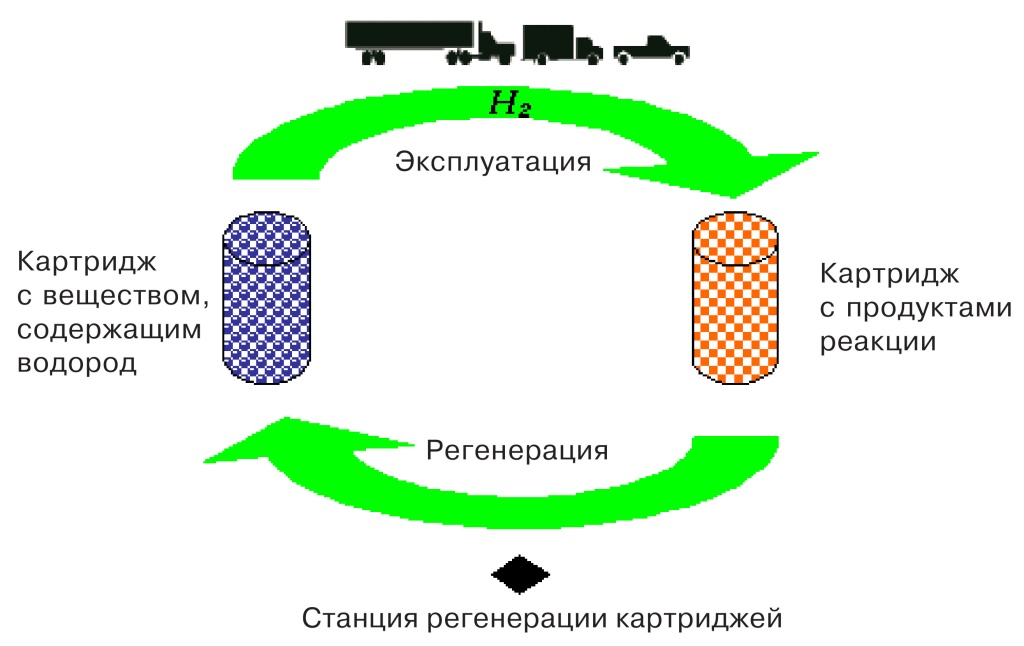 |
| Схема использования водородных картриджей |
Конечно, сегодня вряд ли можно применить такую схему, например, для автомобилей с двигателем внутреннего сгорания. Ну действительно, зачем нужно создавать картриджи для получения особо чистого водорода, чтобы потом бездумно жечь его в двигателе внутреннего сгорания? Это все равно что взять дорогущий ноутбук последней модели и забивать им гвозди. Гвоздь-то он забьет, но согласитесь, его ведь создали для другого. Что касается картриджей, их следует применять в топливных элементах, работающих с КПД более 70%, где как раз и нужно высокое качество водорода.
