Пути гибели и обновления
В 2016 году Нобелевскую премию по физиологии или медицине присудили профессору Токийского технологического института Ёсинори Осуми за фундаментальные исследования аутофагии — ключевого процесса переработки и реутилизации клеточных компонентов.

|
|
При острой нехватке питательных веществ утилизация не слишком нужных структур, например, хвоста — приемлемая альтернатива! На самом деле Уроборос — более глубокий символ: змей, пожирающий собственный хвост, означает обновление и вечность |
Целительное самопоедание
Слово «аутофагия» до этой премии слышали немногие, но «программируемая клеточная смерть» — не теряющий популярности хит. Цитируя профессора Б.Д.Животовского: «По моим подсчетам, каждые 24 минуты появляется новая публикация, включающая термины “апоптоз”, “некроз”, “аутофагия” или “программируемая гибель клеток”» (см. «Химию и жизнь», 2014, 5). Сейчас трудно вообразить, что еще полвека назад изучение программ, запускающих гибель ненужных или злокачественных клеток, кому-то казалось малоинтересным и что статью, в которой впервые был предложен термин «апоптоз», с трудом приняли к публикации.
Однако апоптоз — лишь один из видов программируемой клеточной смерти. Есть еще программируемая форма некроза (некроптоз) — она играет важную роль в развитии многих серьезных заболеваний, в том числе инфаркта и инсульта. Ороговение, или корнификация, верхнего слоя кожи — оказывается, тоже особый путь клеточной гибели со своей специальной программой. (И в самом деле: почему упомянутый процесс протекает лишь на некоторых участках нашего тела, а на других отмершие клетки незаметно слущиваются?) А четвертый — как раз аутофагия. Хотя это путь не столько смерти, сколько возрождения.
Когда спорят о том, обязательно ли все живое должно стареть и умирать, часто говорят: а вот клетка потенциально бессмертна, амеба или инфузория в благоприятных условиях не стареет и не умирает, а делится, и это происходит бесконечно, на протяжении сотен веков, значит... Не будем разбирать, что это значит для нас, многоклеточных, и чем отличается наше положение от положения амебы, а зададимся вопросом: почему она не стареет? Или для нее не писан второй закон термодинамики? Цепочки должны рваться, активные формы кислорода — окислять биомолекулы, и что делать, чтобы система не пришла в негодность?
Хрестоматийный ответ: живые объекты противостоят энтропии, получая энергию извне и употребляя ее для роста и развития, а также для замены и ремонта поврежденных структур. Один из механизмов клеточного ремонта исследовал нобелевский лауреат 2016 года.
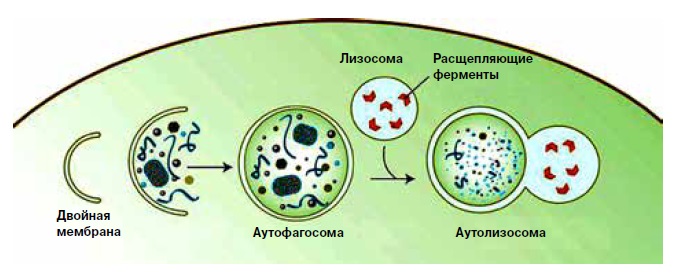
В середине ХХ века электронная микроскопия позволила ученым узнать много нового об устройстве клетки и ее повседневной жизни. Результаты, полученные в то время, имели огромное значение, им воздается должное до сих пор. Всего три года назад, в 2013м, Нобелевскую премию по физиологии и медицине присудили за открытие везикулярного транспорта — точно срежиссированных «перевозок» различных веществ в мембранных пузырьках, как по маршрутам внутри клетки, так и за ее пределы (см. «Химию и жизнь», 2013, 11). А вот бельгийский ученый Кристиан Де Дюв получил свою Нобелевскую премию сравнительно рано, в 1974 году, вместе с Джорджем Паладе и Альбером Клодом «за открытия важнейших клеточных структур». Сам Де Дюв открыл лизосому — клеточный утилизатор, мембранный пузырек с ферментами, расщепляющими биомолекулы. И уже в 50—60е годы были пойманы интересные микроскопические кадры: лизосомы, внутри которых находятся цитоплазма, фрагменты клеточных структур, а иногда целые органеллы, например митохондрии. Был описан также своеобразный механизм доставки этих фрагментов к месту демонтажа: их затягивает в двухслойный мембранный пузырек — аутофагосому, который затем сливается с лизосомой. Название «аутофагия» — буквально «самопоедание» — предложил для этого механизма Кристиан Де Дюв. Иногда аутофагию наблюдали в тканях больных или отравленных токсическими агентами животных, но иногда и в норме — например, во время эмбрионального развития. Она обнаружилась у самых разных животных, от амебы и эвглены до позвоночных. Это означало, что механизм древний и, вероятно, очень важный.
|
|
Схема аутофагии
|
К слову, в 70—80е годы был исследован другой механизм демонтажа ненужных структур — специфическая деградация белков, к которым прикреплен маленький белок убиквитин, точнее, полимер из нескольких убиквитинов. Белки с убиквитиновой меткой направляются в протеасому (крупный, мультисубъединичный белковый комплекс), где расщепляются на аминокислоты. За это открытие Аарон Цихановер, Авраам Хершко и Ирвин Роуз получили Нобелевскую премию по химии 2004 года.
Но протеасомная система утилизирует отдельные молекулы, аутофагия же — утилизация целых белковых комплексов и органелл. Как управляется этот потенциально опасный для клетки процесс? Что запускает образование аутофагосомы? Насколько важна аутофагия для нас и других существ, могут ли ее нарушения быть причиной болезней и если да, то каких? От первых наблюдений аутофагии до первых ответов на эти вопросы прошло несколько десятилетий. Вероятно, иначе и быть не могло: для этого необходимы были эффективные методы исследования генома.
 |
|
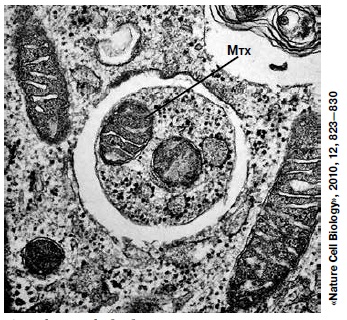
Аутофагия в фибробластах мыши, выращенных на бедной питательными веществами среде. Хорошо видна митохондрия (Мтх) внутри аутофагосомы |
Переполнение мусорного бака
Ёсинори Осуми родился в 1945 году в городе Фукуока. Отец его был профессором инженерных дисциплин в университете Кюсю, но Осуми-младший больше интересовался естественными науками, чем техникой. Он поступил в Токийский университет, чтобы стать химиком, однако вскоре понял, что эта наука не так уж сильно его привлекает — в ней, как ему казалось, мало новизны. «Но, думаю, мне повезло, — говорил он в интервью «Journal of Cell Biology» 2012 года, — потому что начало 60-х было золотым веком молекулярной биологии. Я решил, что хочу заниматься ей».
Во время диплома Осуми изучал синтез белков у кишечной палочки, но выдающихся результатов не получил. Молекулярнобиологических лабораторий в Японии того времени было не так много, найти работу казалось сложно. Получив степень в 1974 году, Осуми отправился в США — в Рокфеллеровский университет, где стал постдоком у нобелевского лауреата Джеральда Эдельмана. Там ему пришлось переключиться на биологию развития млекопитающих, и он вспоминает об этом периоде без восторга. Но именно в лаборатории Эдельмана он приобрел опыт работы с дрожжами Saccharomyces cerevisiae, который пригодился ему впоследствии.
Вернувшись в альма-матер, доктор Осуми выбрал темой исследований вакуоли дрожжей. «В то время многие изучали транспорт ионов и небольших молекул через плазматическую мембрану, но мало кто брался изучать транспорт через мембраны органелл. А вакуоль (функциональный аналог лизосомы многоклеточных. — Примеч. ред.) считали просто мусорным баком клетки, не очень-то много людей интересовались ее физиологией, и я подумал, что было бы неплохо исследовать транспорт в вакуоли, поскольку у меня будет мало конкурентов». Действительно, в этой области ему сопутствовала удача. В 1988 году 43-летний Осуми стал руководителем группы — не сказать чтобы звездная карьера. И он решил исследовать литическую функцию вакуоли, ее способность переваривать биомолекулы.
Дрожжи — один из самых популярных экспериментальных объектов. С одной стороны, они эукариоты, имеют ядро и прочие органеллы, то есть гораздо больше похожи на нас, чем, например, бактерии. С другой стороны — они сравнительно просто устроены и быстро размножаются, их несложно культивировать, что подтверждает многовековой опыт человечества по приготовлению спиртных напитков.
Неудобны дрожжи тем, что их клетки довольно малы: их типичный размер исчисляется микрометрами, крупнее кишечной палочки, но меньше большинства эукариотических клеток. Было даже не очень понятно, есть ли у них аутофагия. Осуми исходил из предположения, что есть и должна усилиться у голодающих клеток (они будут демонтировать наименее нужное, чтобы получить энергию для выживания). А если у этих клеток ферменты, отвечающие за деградацию молекул, будут повреждены мутацией, то процесс переваривания застопорится и клеточное несварение должно стать заметным.
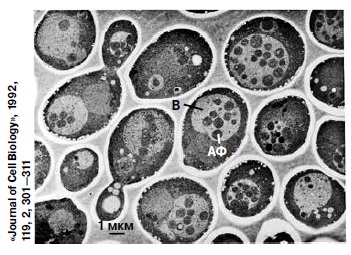
Итак, штаммы дрожжей, не имеющие протеиназы А, протеиназы В и карбоксипептидазы, стали выращивать на среде, бедной питательными веществами. Рассматривать клетки под микроскопом Осуми нравилось, наблюдения он вел сам. «Через 30 минут голодания появилось множество пузырьков и они начали накапливаться в вакуоли. У меня был хороший знакомый — специалист по электронной микроскопии, и мне посчастливилось наблюдать образование аутофагосом и их слияние с вакуолью. Это стало отправной точкой моей работы...» Действительно, на фото хорошо видны мелкие пузырьки в вакуолях, которые не деградируют («Journal of Cell Biology», 1992, 119, 301—311). Таким образом, стало ясно, вопервых, что аутофагия у дрожжей имеет место, а во-вторых — как выглядит клетка, у которой аутофагия затормозилась на последнем этапе.
|
|
Дрожжевые клетки с дефектными ферментами, выращенные на голодной диете: в вакуолях (В) накапливаются пузырьки аутофагосом (АФ) |
От микроскопии к генетике
Почему важно это «во-вторых» — замечательно объяснил Юрий Лазебник в эссе 2002 года «Может ли биолог починить радио?». (Кстати, и он в свое время исследовал апоптоз в знаменитой лаборатории Колд-Спринг-Харбор.) Он предлагает читателям вообразить биологов, изучающих транзисторный радиоприемник теми же методами, которыми они изучают гены и белки живой клетки, причем допускает правдоподобное предположение, что физике и радиотехнике биологи не обучены. Для начала надо раздобыть денег и купить много одинаковых радиоприемников, научиться их вскрывать, затем описать и классифицировать найденные внутри компоненты — по форме, цвету, размеру и количеству ножек. «Более эффективным окажется подход, согласно которому компоненты поочередно удаляют, или вариант, когда в радио стреляют с близкого расстояния металлическими частицами. В последнем случае те приемники, которые сломаются (произведут "фенотип"), будут отобраны, чтобы понять, поломка какой детали привела к такому фенотипу. Хотя удаление большинства компонентов будет давать лишь незначительный эффект, какой-нибудь везучий постдок случайно найдет проводок, отсутствие которого полностью прекратит музыку. Ликующий ученый назовет проводок Удачно Расшифрованным Компонентом (УРК), после чего узнает, что УРК является единственным связующим звеном между длинным выдвигающимся объектом и остальными частями приемника...»
История борьбы биологов с радиоприемником длинна и забавна, а мораль ее в том, что биологам стоило бы позаимствовать коекакие подходы и методы описания сложных систем у инженеров. Но пока биосистемы не стали для нас такими же ясными, как схемы электроприборов, остается полезным умение ломать радиоприемники. В особенности так, чтобы удавалось связать поломку (отошел контакт) с нарушением конкретной функции (искажаются высокие звуки).
Вот почему дрожжевые клетки с вакуолями, набитыми пузырьками, были настоящим сокровищем. Дальше исследователи рассуждали так: если у штамма с дефектом переваривания аутофагосом появится еще одна мутация и при этом в условиях голодания прекратится появление вакуолей с пузырьками, значит, продукт мутантного гена задействован в аутофагии. (Мы видим, что будущий нобелевский лауреат использовал немного более хитрый способ, чем традиционный: нашел поломку, которая делала более заметными другие поломки.)
Поиском этих генов и занялась в 90-е годы группа Осуми, на тот момент состоявшая из трех человек — самого доктора и двух студентов. Дрожжевые штаммы подвергали химическому мутагенезу, чтобы получить случайные мутации, а затем индуцировали в них аутофагию и смотрели, как изменится фенотип. Студентке Осуми Мики Цукада удалось обнаружить первый ген аутофагии, который, естественно, назвали APG1 (autophagy gene; в настоящее время этим генам присвоена аббревиатура ATG). У дрожжей — носителей мутации не начиналась аутофагия во время голода, и они быстро теряли жизнеспособность, поскольку у них был перекрыт резервный источник энергии и строительного материала.
Очень скоро Осуми с коллегами обнаружили у дрожжей целых 15 генов аутофагии («FEBS Letters», 1993, 333, 169—174), а также охарактеризовали их белки. Примерно в то же время был опубликован геном дрожжей, что сильно упростило работу.
Прояснилось и с регуляцией. Так, белок Atg1 принадлежит к семейству киназ, то есть фосфорилирует белки (регуляция с помощью фосфатной метки широко распространена в природе). Он взаимодействует с продуктом ATG13, и это взаимодействие регулируется знаменитой киназой — мишенью рапамицина (TOR), которая участвует в контроле роста, старения и ответа на стрессы. Она активна в клетках, когда те хорошо питаются, и фосфорилирует Atg13, чем предотвращает его взаимодействие с Atg1. Голодание же инактивирует TOR, нефосфорилированный Atg13 связывается с Atg1, и запускается аутофагия. А потом выяснилось, что при этом образуется пентамерный комплекс, из пяти белков — Atg13, Atg1, Atg17, Atg29, Atg31... Все, о чем мы только что рассказали, — лишь первый шаг в каскаде событий, необходимых для формирования аутофагосомы, которая в итоге заключит в себя фрагмент клеточной структуры, назначенный к уничтожению.
Конечно, всех интересовало, существуют ли аналогичные механизмы у других живых существ. Осуми с коллегами первыми нашли такие гены у млекопитающих (например, мыши, дефектные по ATG5, нормальны при рождении, но умирают в первый же день жизни, неспособные перетерпеть перерывы между кормлениями). Есть они и у человека, причем механизм очень похож на тот, что был открыт у дрожжей.
Истребление всего ненужного
Сегодня мы знаем об аутофагии сравнительно много. Деградацию крупных порций цитоплазмы и клеточных органелл, то, что, собственно, наблюдал Осуми, называют макроаутофагией. Неселективная аутофагия в клетке происходит постоянно, обеспечивая обновление структур, и усиливается в ответ на стресс. Но бывает аутофагия и селективной — когда белковые агрегаты, органеллы, вирусы или бактерии, которых надо уничтожить, несут специфическую метку. Уничтожение проникших в клетку бактерий и вирусов имеет отдельное название — ксенофагия, исследование этого процесса и того, как некоторые возбудители заболеваний научились с ним бороться, — особая тема. Есть также микроаутофагия (лизосома «заглатывает» маленькие порции цитоплазмы) и шаперон-опосредованная аутофагия отдельных белков — в отличие от убиквитиновой системы, которая утилизирует главным образом короткоживущие белки, более не нужные, аутофагия удаляет долгоживущие.
Аутофагия участвует также в эмбриональном развитии и дифференциации клеток. Ее дефекты наблюдаются при болезни Паркинсона, различных нарушениях развития мозга, эпилепсии, диабете второго типа, некоторых видах рака (рак груди и яичников часто может быть связан с мутацией в гене BECN1, гомологе дрожжевого ATG6). Интересно, что среди противораковых препаратов есть как стимуляторы аутофагии, так и ее блокировщики. Первые предотвращают развитие опухоли, вторые применяются, если рак уже прогрессирует, чтобы раковые клетки не использовали аутофагию как механизм устойчивости к химиотерапии. С нарушениями в генах аутофагии связаны некоторые наследственные заболевания, например синдром Вици.
Вместо заключения приведем рекомендацию Ёсинори Осуми для ученых, карьера которых складывается не слишком благоприятно, как у него самого поначалу (из того же интервью 2012 года, когда он еще не знал, что станет нобелевским лауреатом, но уже достиг значительных успехов): «К сожалению, сегодня, по крайней мере в Японии, молодые ученые хотят получить стабильную работу, поэтому боятся рисковать. Большинство предпочитает работать в самых популярных областях, думая, что это простейший способ опубликоваться. Но я сделал наоборот. Я не очень люблю конкурентную борьбу, поэтому всегда искал новые предметы для изучения, пусть даже не слишком популярные. Если вы начнете с базовых, новых наблюдений такого рода, у вас будет уйма работы»
