Новые ощущения
Лауреатами Нобелевской премии по физиологии или медицине 2021 года стали Дэвид Джулиус (США, Калифорнийский университет Сан-Франциско) и Ардем Патапутян (Ливан — США, Институт Скриппс) «за открытие рецепторов температуры и прикосновения». Дэвид Джулиус использовал капсаицин, жгучее вещество перца, чтобы обнаружить ионный канал в нервных окончаниях кожи, который реагирует на высокую температуру. Ардем Патапутян открыл новый класс датчиков, реагирующих на прикосновение и давление в коже и внутренних органах.
 |
|
Ардем Патапутян открыл рецепторы, которые обеспечивают восприятие прикосновения.
Фото: UPI / Alamy / TASS
|
Ричард Фейнман в «сумасшедшей ванне»
Мы недооцениваем осязание. Оно кажется менее важным, чем зрение или слух, которые необходимы для общения и ориентации в пространстве. Нет, конечно, полезно вовремя ощутить боль, а удовольствие от поглаживаний закрепляет социальные связи… На самом деле у осязания функция менее заметная, но крайне важная. Это интерфейс между нами и миром, всего-навсего.
Станислав Лем в одном из рассказов о пилоте Пирксе описывает тестирование будущих пилотов космических кораблей. Среди испытаний было и такое, на первый взгляд нестрашное: «Испытуемый — на студенческом жаргоне “пациент” — раздевался и погружался в воду, которую нагревали, пока он не терял ощущение температуры. Это было индивидуально: для одних вода “переставала существовать” при двадцати девяти градусах, для других — лишь после тридцати двух. Когда юноша, лежавший навзничь в воде, поднимал руку, воду прекращали нагревать, и один из ассистентов накладывал ему на лицо парафиновую маску. Затем в воду добавляли какую-то соль (…) Ее сыпали, пока “пациент” (он же “утопленник”) не всплывал так, что тело его свободно держалось в воде чуть пониже поверхности. Металлические трубки высовывались наружу, и он мог свободно дышать.
Вот, собственно, и все. На языке ученых этот опыт назывался “устранение афферентных импульсов”. И в самом деле, лишенный зрения, слуха, обоняния, осязания (…) “утопленник”, скрестив руки на груди, покоился в состоянии невесомости. Сколько времени? Сколько мог выдержать. Как будто ничего особенного. Однако с человеком начинало твориться нечто странное...»
В рассказе Лема переживания «утопленников» были разнообразными, но всегда неприятными: распад собственного «я», галлюцинации, панические атаки. Считалось, что пережитый экзистенциональный ужас подготовит курсантов к одиночеству в космическом пространстве и покажет, кто чего стоит. Юный Пиркс, продержавшись в «сумасшедшей ванне» семь часов, поразил врача и получил крайне необычное задание, но это уже другая история.
Лем, как это ему свойственно, использовал факты из научной литературы своего времени. Камеру сенсорной депривации в 1954 году построил Джон Лилли, врач, психолог и психоаналитик, чьи идеи сейчас кажутся несколько эксцентричными, но в середине ХХ века производили грандиозное впечатление. В реальности этот опыт далеко не для всех был неприятным, но все отмечали, что ощущения весьма странные, подходящие под определения «измененного сознания». В «сумасшедшей ванне» лежал даже умница и скептик Ричард Фейнман. Галлюцинаций у Фейнмана, к его огорчению, не было ни в первый, ни во второй раз, но, когда он испробовал дыхательные упражнения, которым его научил «парень из Гарварда, который ездил в Индию», началось: «На каком-то этапе игры я внезапно осознал — это сложно объяснить, — что я сдвинулся на дюйм в сторону. Другими словами, мое дыхание, вдох и выдох, вдох и выдох, происходит не в центре: мое эго слегка сдвинулось в одну сторону, примерно на дюйм».
То поколение ученых питало огромный интерес к химическим галлюциногенам. Сам Фейнман не решался их пробовать («я люблю думать и не хочу портить машину, которая помогает мне в этом»), но галлюциноген физический, разрешенный во всех штатах, его увлек. О том, что он видел, можно прочитать в книге «Вы, конечно, шутите, мистер Фейнман!» — какой мозг, такие и галлюцинации. Разумеется, он пытался вызвать у себя это состояние без ванны, просто сидя на удобном стуле. И разумеется, ничего не вышло.
Надеюсь, теперь достижения нобелиатов 2021 года видятся иначе. Не просто «какие-то рецепторы в коже», как говорили некоторые непросвещенные комментаторы, а фундамент нашего самоощущения, ощущения себя в мире. Тепло, холод, мягкость и жесткость, давление, боль — понятия основополагающие, язык, на котором говорит с тобой мир еще до того, как ты выучишь слова человеческой речи. Все это настолько простые вещи, что о них трудно думать, они просто есть.
А если мы попытаемся подумать, то поймем, что осязание — вовсе не «одно из пяти чувств». Чувствительность к температуре, прикосновению, давлению и боли — минимум четыре разных чувства. (На самом деле еще больше.) Жестяная коробочка с гайками может быть тяжелой, гладкой и холодной, и это три независимых характеристики, можно утратить одну из них и сохранить две других. Высыплем гайки, и коробочка станет легкой, хотя останется гладкой и холодной; ошкурим краску — она станет шершавой, оставим на солнце — она перестанет быть холодной и будет теплой. С другой стороны, давление, холод или жар могут причинять боль.
Еще Рене Декарт, описывая предполагаемое устройства машины человеческого тела, выдвинул гипотезу, что от обожженного участка кожи в мозг по нервам (Декарт считал их трубочками) устремляются «животные духи» — особые частицы, которые «очень малы и движутся очень быстро, подобно частицам пламени, вылетающим из огня свечи», и обеспечивают все функции живого тела. Затем «животные духи» направляются к мышцам конечности и раздувают их, заставляя сокращаться — человек отдергивает руку. Нам, учившим в школе про нейроны и синапсы, смешно, однако эта «стимпанковская» модель нервной реакции была довольно глубокой — например, из нее следовало, что реакция отдергивания руки от горячего осуществляется механически, без участия мозга; в модели Декарта она отделена от осознания и переживания боли. И.П. Павлов был большим поклонником Декарта.
Сейчас мы знаем, что «животные духи», передающие сигнал по нервам, — это стремительное перераспределение зарядов на мембране нейрона, вызванное открытием специальных каналов для ионов в этой мембране. Нейроны, в свою очередь, принимают сигналы от рецепторов. У нас есть рецепторы для детекции сильного давления; легкого прикосновения и текстуры поверхности (с их помощью мы читаем брайлевский шрифт); продолжительности давления, формы краев предметов, растяжения кожи; прикосновения к волоскам… Есть специализированные рецепторы довольно сложного строения, но есть и просто свободные нервные окончания в толще эпителия, которые воспринимают температурные и механические воздействия, а также боль.
Дэвид Джулиус и Ардем Патапутян в 2020 году стали лауреатами престижной премии Кавли. Эта премия, учрежденная норвежским филантропом Фредом Кавли, вручается раз в два года, начиная с 2008-го, за исследования в области астрофизики, нанотехнологий и нейронаук («за самое большое, самое маленькое и самое сложное»). Было замечено, что иногда премия Кавли становится «репетицией» Нобелевской премии. Так, лауреаты прошлого года, пионеры CRISPR-Cas Дженнифер Дудна и Эммануэль Шарпантье получили премию Кавли в 2018 году вместе с Виргиниюсом Шикшнисом из Вильнюсского университета. На сайте этой премии размещены автобиографии лауреатов, поэтому нам не нужно ждать, когда они появятся на нобелевском сайте: прочитать рассказы об открытиях, написанные ими самими, мы можем уже сейчас.
Чай с мятой и мороженое с перцем
Мы говорим «перец жжет», «мята холодит» и думаем, что употребляем эти слова в переносном смысле, ведь и перец, и мята на самом деле комнатной температуры. Так вот, никакого переносного смысла. Жжение перца и мятный холодок мы воспринимаем благодаря тем же самым механизмам, что высокую и низкую температуру.
Американский нейробиолог Дэвид Джулиус родился в 1955 году. Он вырос в Бруклине, штат Нью-Йорк, в районе на побережье Атлантического океана, название которого много говорит русскому уху: Брайтон-Бич, любимое место поселения иммигрантов из Восточной Европы. Бабушки и дедушки Джулиуса, как он пишет, уехали в Соединенные Штаты от антисемитизма царской России. Родители стали американцами в первом поколении: отец — инженер-электрик в телефонной компании, мать — учительница начальной школы. В 1977 году Джулиус получил степень бакалавра в Массачусетском технологическом институте. Увлеченный научными исследованиями, он отказался от занятий практической медициной и защитил диссертацию (PhD) по биохимии пептидных гормонов в Калифорнийском университете в Беркли. Предметом его постдокторского исследования были рецепторы нейромедиатора серотонина; тогда он и заинтересовался сенсорными нейронами, которые передают ощущения в мозг.
Естественно, в те времена и в тех местах молодой ученый не мог избежать интереса (чисто академического) к галлюциногенам и другим природным биоактивным соединениям. Всем было любопытно, но у биохимиков и молекулярных биологов интерес был профессиональный. Хотелось с декартовой дотошностью разобрать механизм действия «расширителей сознания», а потом использовать их как лекарства — или орудия для исследования. Новые методы манипуляций с генами давали такую возможность. «Сошлись два потока мыслей: мое сосредоточение на превращениях феромонов заставило меня задуматься о молекулярных и физиологических действиях гормонов и нейромедиаторов в головном мозге; и, возможно, под влиянием истории берега залива Сан-Франциско я был очарован фармакологией галлюциногенов, опиатов и других натуральных продуктов, которые общества тысячелетиями использовали для изменения сознания и сенсорного опыта», — пишет Джулиус.
«Сенсорный опыт» в дальнейшем стал главным. Джулиус прочитал работы венгерских и других ученых, в которых было показано, что некоторые сенсорные нейроны становятся активным в присутствии как тепла, так и капсаицина, «горячего» ингредиента перца. В Венгрии к перцу всегда относились трепетно. Заинтересовал он и Джулиуса.
Капсаицин (8-метил-N-ванилил-6-ноненамид) — то самое вещество, от которого слезы льют из глаз, если перепутаешь молотый перец чили с молотой паприкой. Если капсаицин активирует нейроны, значит, он взаимодействует с какими-то каналами, пропускающими ионы (мы помним, что нервный импульс связан с зарядом на мембране). И найти эти каналы важно не только для глубинного понимания вкуса гуляша: они могут опосредовать также тепло и боль, а это уже серьезно. Во второй половине 1990-х годов Дэвид Джулиус, уже в Калифорнийском университете Сан-Франциско, начал поиски рецептора капсаицина.
У каждого белка есть ген, и его можно найти. Джулиус и его коллеги создали библиотеку комплементарных ДНК из спинальных ганглиев грызунов — известно было, что именно там находятся сенсорные нейроны, активируемые капсаицином. (Комплементарные ДНК, или кДНК — ДНК-копии матричных РНК, то есть «восстановленные» гены всех белков, которые синтезируются в данной клетке. Создать библиотеку кДНК из определенных клеток — это как получить доступ к статистике скачиваний файлов из огромного книжного магазина, увидеть, какие книги наиболее популярны, и вычислить бестселлер — ген того самого рецептора, который обязан быть в этих клетках.) Полученные кДНК внедряли в клетки, нечувствительные к капсаицину, и однажды после трансформации очередным геном они стали чувствительными к нему. Ген был найден.
Изучив последовательность гена, можно сделать вывод о свойствах белка, который кодирует этот ген. Как и предполагалось, это был ионный канал — «ворота» в мембране нервной клетки, которые открываются при связывании с определенным веществом, в данном случае с капсаицином. Белок принадлежал к семейству так называемых каналов с транзиторным ионным потенциалом (TRP), которые обеспечивают чувствительность к различным стимулам, от света до химических веществ. Каналы этого семейства ранее находили у дрозофил, но у млекопитающих его функцию установили впервые. Белок, который открыли Джулиус с коллегами в 1997 году, получил название TRPV1.
Действительно, TRPV1 активировался под действием тепла. Точнее, жара: порог его активации превышает 43°C, что близко к психофизическому болевому порогу. Этот белок синтезируется в ноцицептивных нейронах (отвечающих за восприятие боли), но не в нейронах, участвующих в восприятии положения тела, прикосновения и давления. Помимо высоких температур или капсаицина, канал TRPV1 включается высокой концентрацией протонов в ишемизированных тканях и химическими соединениями, которые образуются во время воспаления. Иными словами, это рецептор воспаления. У мутантных мышейс дефицитом TRPV1 снижается не только тепловая чувствительность, но и чувствительность к боли, вызванной воспалением или онкозаболеванием.
У животных, лишенных гена TRPV1, чувствительность к обжигающему теплу не исчезала. Значит, должны быть и другие рецепторы, активируемые температурой, и в 2011 году другая группа исследователей открыла TRPM3 — еще один датчик вредного тепла. Канал TRPA1, открытый в 2004 году независимо лабораториями Джулиуса и Патапутяна, знаменит как «рецептор васаби», но реагирует также на горчичное масло, чеснок и различные химические раздражители. У разных видов животных этот канал активируется различными температурами и разными химическими веществами. А его активация веществом, вырабатываемым при остеоартрите, вносит вклад в восприятие боли.
Кроме чувства тепла, у нас есть и чувство холода, с отдельным рецептором. Лаборатории Дэвида Джулиуса и Ардема Патапутяна в 2002 году открыли, тоже независимо друг от друга, рецептор TRPM8, который активируется ощущением приятной прохлады — ниже 28°С. Для его идентификации использовали ментол, следуя той же логике, что и с капсаицином.
Таким образом, за восприятие горячего и холодного отвечает целый оркестр кожных рецепторов. По современным представлениям, ионные каналы TRPV1, TRPA1, TRPM2 и TRPM3 вместе действуют как сенсоры тепла, но тепло надежно воспринимается только тогда, когда оно подавляет активность «холодного» TRPM8. Если интересно, поэкспериментируйте с мятной зубной пастой и теплой водой.
Кстати, года три назад огромной популярностью пользовалось мороженое с перцем, в сотни раз острее, чем соус табаско, по заявлению производителей. Если TRPV1 активирован капсаицином, его инактивирует — кто бы мог подумать! — холод. Поэтому адский десерт можно спокойно держать во рту. Правда, когда мороженое проглочено, рецептор активируется снова и гарантирует потребителю незабываемые впечатления. Многим нравится.
Джулиус и его коллеги идентифицировали TRPV1 и его родственников в инфракрасных «датчиках» летучих мышей и змей. Кроме того, эти каналы являются мишенями токсинов пауков и скорпионов — то самое жжение в месте укуса.
Для включения нажать
Ардем Патапутян родился в Бейруте в 1967 году. «Моя мама была учительницей и директором начальной школы, а мой отец — писателем и бухгалтером. Я был младшим из троих детей, мне было восемь лет, когда началась гражданская война в Ливане, — вспоминает он. — Жизнь часто была по понятным причинам напряженной, с комендантским часом, ограниченными часами электричества и нередкими взрывами. Нас, армян, обычно воспринимали как квазинейтральную сторону в борьбе христиан с мусульманами, и мы посещали небольшие армянские школы, размер классов в которых продолжал сокращаться по мере того, как все больше семей спасалось от войны. К моему первому году в старшей школе нас осталось всего пять учеников, все мои дорогие друзья». В следующем году школа закрылась, Ардема устроили в «мультикультурную» частную школу с высокими требованиями; сначала было трудно, но потом у мальчика обнаружились способности к математике и естествознанию. Ардем в течение года посещал курсы бакалавриата в Американском университете в Бейруте. Однако конфликт продолжал нарастать, однажды Ардем даже попал в плен к боевикам. Через несколько месяцев после освобождения он переехал в Лос-Анджелес.
Это был 1986 год. Начало в Соединенных Штатах было нелегким: будущий нобелевский лауреат писал гороскопы для местной армянской газеты. Но потом поступил в Калифорнийский университет Лос-Анджелеса, диссертацию сделал в Калтехе, затем работал в Калифорнийском университете Сан-Франциско — совсем недалеко от Джулиуса, который клонировал ген TRPV1.
Ардем Патапутян создал свою лабораторию в Институте Скриппс (Ла-Хойя, Калифорния, США) и начал искать механочувствительные каналы — те, которые реагируют на прикосновение и (или) сильное давление.
Еще в конце 1980-х годов механочувствительные ионные каналы обнаружили у кишечной палочки Escherichia coli — бактериям они помогают приспособиться к снижению осмотической концентрации среды и не лопнуть. Обнаружение механочувствительного ионного тока в нейронах спинальных ганглиев крыс подтвердило, что где-то в них такие каналы есть. Однако их не удавалось найти, пока Ардем Патапутян не предложил новый подход к скринингу. Это произошло в 2010-е годы.
Патапутян вместе с докторантом Бертраном Косте впервые обнаружили механочувствительную линию клеток Neuro2A (это были клетки мышиной нейробластомы, которые используются как модель нервной ткани). Клетки продуцировали электрический сигнал в ответ на короткое надавливание кончиком микропипетки. Ученые проанализировали экспрессию генов в этих клетках. Генов белков, которые могли оказаться неизвестными ионными каналами, набралось 72.
Эти гены инактивировали один за другим с помощью РНК-интерференции. За открытие этого механизма в 2006 году тоже дали Нобелевскую премию: небольшая молекула РНК связывается с матричной РНК определенного гена и отправляет ее на уничтожение, в результате белок не синтезируется. Когда ДНК-интерференцию проводят в эксперименте, это называют генным нокдауном: в отличие от нокаута, когда необратимо повреждается участок ДНК, содержащий ген, РНК-интерференция отключает ген временно.
Нокдаун последнего гена из 72-х, ранее известного как FAM38A, лишил клетки способности реагировать на нажатие. Новый механочувствительный ионный канал, кодируемый этим геном, получил название PIEZO1, от греческого слова, обозначающего давление. (От того же слова происходит «пьезоэлектричество», заряд, возникающий от нажатия на кристалл, в зажигалке или электроподжиге газовой плиты.) По сходству с PIEZO1 был открыт ген второго канала — PIEZO2. Они принадлежали к новому, ранее неизвестному семейству белков.
Как выяснилось в следующем десятилетии, PIEZO2 участвует в восприятии легких прикосновений. В коже человека и животных, особенно в высокочувствительных участках, есть так называемые клетки Меркеля — овальные клетки в глубинных слоях эпидермиса, к которым подходят нервные окончания. Патапутян с коллегами показали, что в клетках Меркеля краткое прикосновение вызывает PIEZO2-зависимый ток и он, в свою очередь, запускает потенциал действия в нейронах. Однако нейроны обладают собственной механочувствительностью — система дублируется. Но когда в лаборатории Патапутяна создали мышей, у которых отсутствовал PIEZO2 как в клетках Меркеля, так и в сенсорных нейронах, эти мыши оказались невосприимчивы к легким прикосновениям (а вот термочувствительность у них не пострадала).
У людей с мутациями, инактивирующими PIEZO2, нарушены различные аспекты осязания — способность различать текстуру поверхности, восприятие прикосновений и вибрации, чувствительность к прикосновению к волоскам на коже.
Кроме того, PIEZO2 играет ключевую роль в проприоцепции, то есть ощущении положения и движения тела. У мышей без этого канала нарушена координация движений. Каждый, у кого была мышь или крыса, знает, как животное тянется лапами вниз, когда его поднимают за хвост. Мыши с дефицитом PIEZO2 сжимали пальцы в «кулачки» и прижимали лапки к туловищу либо вытягивали их в произвольных направлениях, как будто не понимали, где низ.
Исследования Патапутяна с коллегами и других лабораторий определили структуру каналов PIEZO1 и PIEZO2. Оказалось, что эти белки похожи на трехлопастный пропеллер, вставленный в мембрану клетки и слегка вогнутый. При нажатии на мембрану лопасти пропеллера расправляются, он становится более плоским, и в его центре открывается канал. Простое изящное решение: механическое воздействие превращается в поток ионов, а затем в активацию нервной клетки.
До сих пор мы почти не говорили о тех сигналах, которые идут не от кожи, а от внутренних органов. Каналы PIEZO1 и PIEZO2 регулируют важные физиологические процессы: артериальное давление, дыхание, мочеиспускание. PIEZO2 на рецепторах растяжения легких в стенке бронхов и бронхиол активируются при глубоком вдохе и инициируют рефлекс, защищающий легкие от чрезмерного раздувания (да, в организме нужно предусмотреть и это!). У мышей, лишенных этих белков, наблюдаются гипертензия и скачки артериального давления. Интересно, что PIEZO1 регулирует объем эритроцитов (без него они набирают избыток влаги и разбухают — хочется вспомнить кишечную палочку и ее механочувствительные каналы), а также участвует в ремоделировании скелета через механические нагрузки во время роста.
Современная медицинская генетика выделяет в особую группу каналопатии (chаnnelopathies) — наследственные заболевания, которые вызваны мутациями генов, кодирующих белки ионных каналов. Есть каналопатии, затрагивающие наши «нобелевские» каналы. Каналопатия TRPA1, она же синдром семейной эпизодической боли типа 1, вызывается точечной мутацией (заменой одного нуклеотида) в гене TRPA1. Среди симптомов — изнурительные боли в верхней части тела, которые вызываются холодом, голоданием и физическим напряжением. Другие нуклеотидные замены в этом гене влияют на чувствительность к холоду, теплу или капсаицину.
Мутации с потерей функции в гене PIEZO2 приводят к дистальному артрогрипозу — характерному положению стоп, кистей и пальцев, нарушению проприоцепции и осязания. С возрастом у пациента появляются мышечная слабость, сколиоз и другие нарушения развития скелета. Дефицит интероцептивных ощущений от легких и мочевого пузыря приводит к респираторным расстройствам и нарушениям мочеиспускания. Людям с мутациями, нарушающими функции PIEZO2, бывает трудно передвигаться в темноте. Мутации, усиливающие функцию этого белка, тоже опасны.
Наследственные заболевания вызывают и мутации в гене PIEZO1. Однако Патапутян с коллегами обнаружили интересный пример потенциального эволюционного преимущества, которое может давать мутация в гене этого белка. Одна из мутаций, усиливающих его функцию, вызывает обезвоживание эритроцитов и снижает риск тяжелой инфекции малярийным плазмодием. Этот аллель широко распространен в Африке.
Результаты исследований Джулиуса и Патапутяна не только раскрыли молекулярные механизмы, которые отвечают за восприятия температуры и прикосновения, но и стали основой для разработки методов лечения. В частности, TRPV1 и родственные ему каналы рассматриваются как мишени обезболивающих препаратов. Новые способы избавления людей от боли — это очень важно. Однако не менее важно понять, как функционируют каналы связи между нами и миром. Может быть, когда мы сделаем протез руки с функцией осязания, мы вспомним лауреатов 2021 года.
 |
|
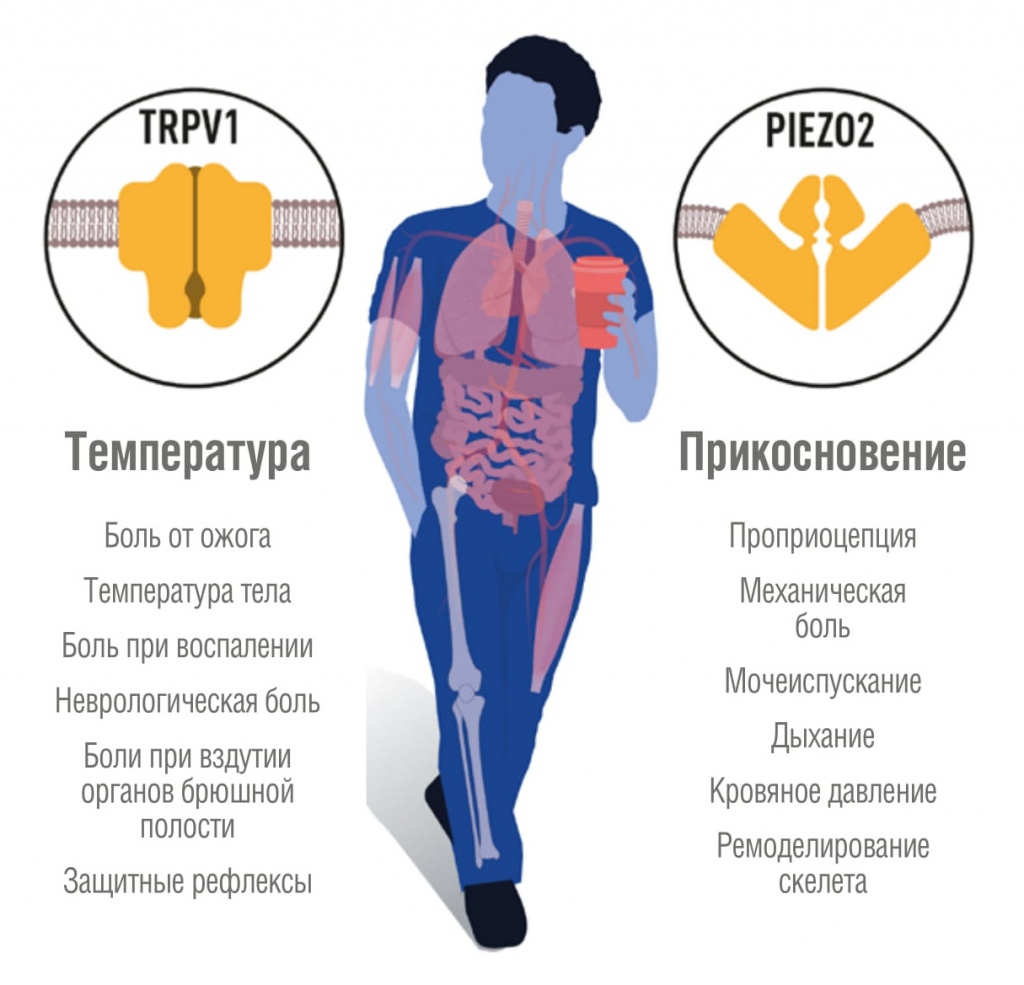
Иллюстрация из пресс-релиза Нобелевского комитета |
