Получать борорганику стало проще
 |
|
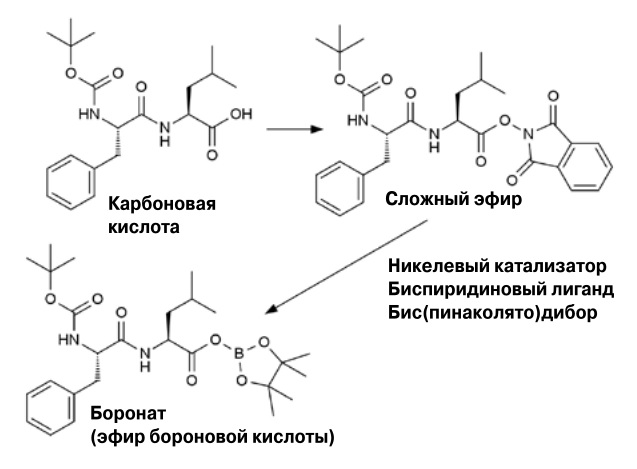
Карбоновую кислоту можно превратить в сложный эфир бороновой кислоты, не выделяя промежуточные продукты реакции |
Химики из группы Фила Барана, работающие в Исследовательском институте Элен Скриппс (Калифорния, США), придумали удобный для лабораторной практики метод превращения карбоновых кислот в эфиры бороновых кислот и сами кислоты («Science», 2017, doi: 10.1126/ science.aam7355).
Благодаря вакантной орбитали бор и многие его производные обладают льюисовской кислотностью и демонстрируют уникальные химические свойства. Например, бороновая кислота и ее эфиры боронаты незаменимы для органического синтеза: их применяют для сборки связи С—С в реакции Сузуки. С их помощью получают функциональные полимеры, лекарства, которые в том числе используются в терапии рака — бортезомиб и иксазомиб. К сожалению, сегодня существует не так много способов синтеза бороновых кислот и их эфиров, и ни один из них нельзя назвать простым.
Новый способ использует кислоты, карбоксильная группа которых связана с первичным, вторичным и третичным атомами углерода. Это может быть карбоксильная группа в составе аминокислот, пептидов и других соединений природного происхождения. Интересно, что метод, предложенный Бараном с коллегами, годится и для случаев, когда с карбоксигруппой конкурируют за реагенты другие группы.
Так, исследователям удалось получить борорганический аналог антибиотика ванкомицина: в молекуле этого вещества много различных функциональных групп и стереоцентров, однако они подобрали такие условия, при которых в реакции участвовала только карбоксильная группа.
Последовательность реакций такова: карбоновую кислоту модифицируют в сложный эфир, который затем в присутствии никелевого катализатора, биспиридинового лиганда и бис(пинаколято) дибора вступает в реакцию, приводящую к образованию целевых бороновых эфиров. Обе реакции проходят в режиме one pot — без выделения и очистки промежуточных продуктов. Эфиры бороновых кислот можно потом гидролизовать до соответствующих кислот.
Чтобы еще раз продемонстрировать эффективность предложенного подхода, исследователи из группы Барана объединили усилия с Калифорнийским институтом биомедицинских исследований и получили борсодержащие аналоги ингибиторов нейтрофилэластазы человека. Фермент нейтрофилэластаза — важная молекулярная мишень при лечении ряда заболеваний легких, в том числе муковисцидоза. Специалисты Калифорнийского института биомедицинских исследований попытались улучшить ингибиторы нейтрофилэластазы, показавшие низкую эффективность во второй фазе клинических испытаний. Когда в состав этих молекул ввели по методологии Барана борсодержащие фрагменты, полученные соединения оказались более активными ингибиторами, чем их предшественники. Калифорнийский институт биомедицинских исследований планирует изучить их активность in vivo.
