Двое свободных от ВИЧ
В первых числах марта 2019 года ведущие научные журналы и СМИ всего мира опубликовали сообщения о том, что уже второй человек в мире излечился от вируса иммунодефицита. Первым был знаменитый «берлинский пациент», его история началась почти 12 лет назад, и он до сих пор здоров. Второго называют «лондонским пациентом»; авторы статьи в «Nature», где рассказывается об этом случае, пока говорят не о выздоровлении, а о «длительной ремиссии», но ремиссия продолжается уже полтора года.
С начала года исследовательская медицина принесла не одну хорошую новость. Война с «неизлечимыми» заболеваниями не закончится, вероятно, никогда, но мы отвоевываем у врагов жизнь за жизнью. В марте завершила вторую фазу клинических испытаний терапевтическая вакцина против папилломавирусов, вызывающих рак шейки матки, — три укола в бедро обращают вспять предраковые поражения у каждой третьей женщины. В апреле сообщили о хороших результатах генной терапии тяжелого комбинированного иммунодефицита, страшного наследственного заболевания, которое часто называют «болезнью мальчика в пузыре», по имени маленького американца Дэвида Веттера, который прожил 12 лет в стерильной среде. (Обычно дети с таким диагнозом умирают гораздо раньше.) И вот теперь поставлена под сомнение неизлечимость ВИЧ-инфекции.
Про то, как ВИЧ поражает клетку иммунной системы, написаны тысячи исследовательских и популярных статей и даже сделаны анимационные ролики. Мишени вируса — CD4-клетки, то есть клетки, несущие особый белок на мембране — рецептор CD4. Таких клеток много, и они важны для иммунитета, поэтому деятельность вируса — настоящая катастрофа. Поверхностный белок вируса связывается сначала с рецептором CD4, а затем еще с другим клеточным белком, который в этом случае называют корецептором — CCR5 или CXCR4. Только после этого мембраны клетки и вируса сливаются и вирусный геном проникает в клетку. Различают R5-тропные и R5X4-тропные варианты ВИЧ — распознающие или один, или другой корецептор.
 |
|
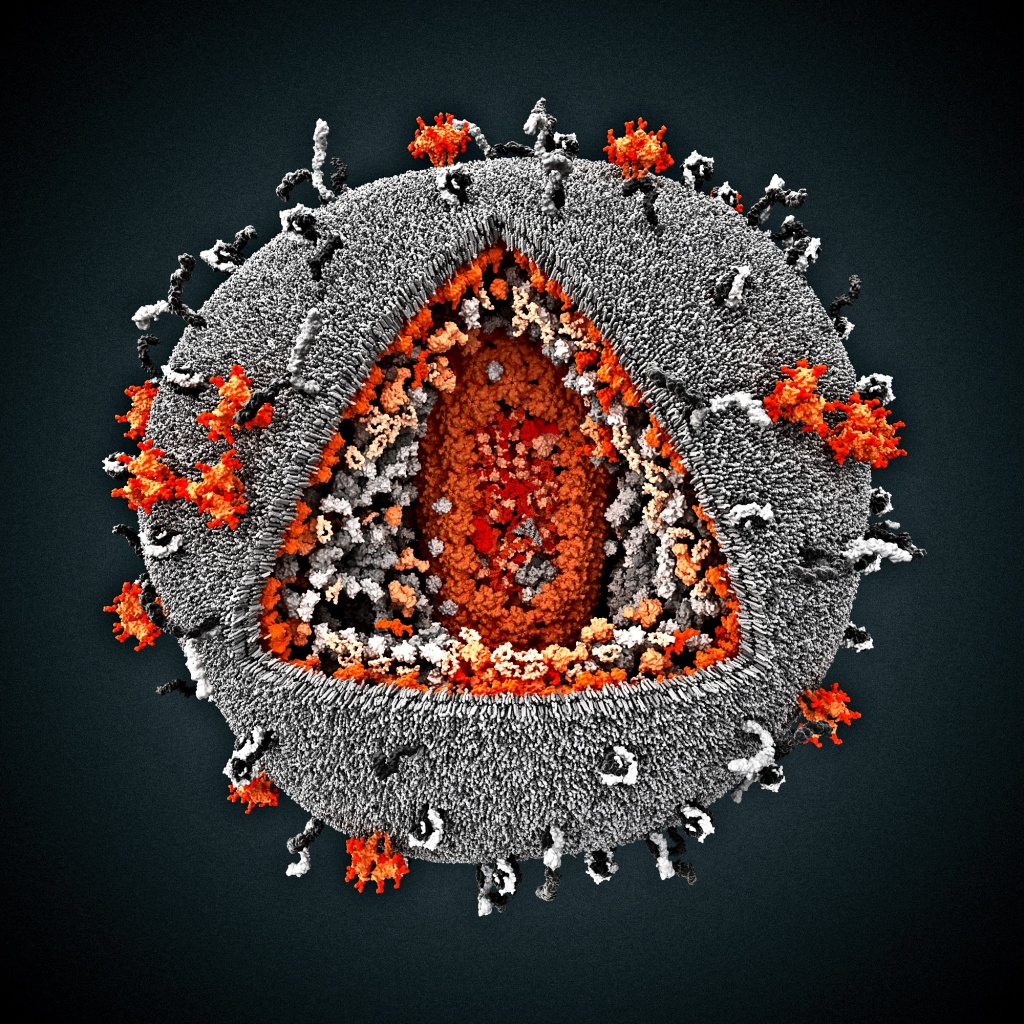
Вирус иммунодефицита человека, Visual Science |
ВИЧ относится к ретровирусам: его генетический материал — РНК, и для дальнейшего развития вируса необходимо выполнить обратную транскрипцию — построить молекулы ДНК на матрице вирусной РНК. (Обычной, «прямой» транскрипцией называют синтез РНК на матрице ДНК.) Делает это вирусный фермент обратная транскриптаза. Затем молекула вирусной ДНК встраивается в геном хозяйской клетки, она начинает производить вирусные белки, собираются новые вирусные частицы, клетка-хозяин погибает, а инфекция распространяется на новые клетки.
В конце концов число CD4-клеток в организме снижается до критического уровня — начинается собственно иммунодефицит. Происходит это небыстро, процесс занимает годы, с длинным латентным периодом. (ВИЧ относится к роду лентивирусов, от латинского lentus — медленный.) В финальной стадии ВИЧ-инфекции для больного становятся опасными любые другие инфекции, в том числе те, что для здоровых практически безвредны; на фоне ослабленного иммунитета могут также развиваться онкологические заболевания.
Таким образом, не каждый ВИЧ-инфицированный болен СПИДом (синдромом приобретенного иммунодефицита), от диагноза до тяжелой болезни есть запас времени. Однако инфицированный пациент, не получающий антиретровирусной терапии, проживет в среднем 10 лет. Хорошая новость в том, что такая терапия существует и обычно позволяет пациенту дожить до старости. Высокоактивная антиретровирусная терапия (ВААРТ) — комбинация нескольких препаратов, каждый из которых подавляет определенную стадию развития вирусов (именно нескольких, чтобы вирус не смог мутировать и приспособиться). Препараты могут препятствовать взаимодействию вируса с рецепторами или его слиянию с клеткой, подавлять вирусную обратную транскриптазу или другой фермент — протеазу, которая особым образом разрезает вирусные белки, чтобы они стали функциональными, или интегразу, которая встраивает вирусную ДНК в геном хозяина. Качество жизни при лечении становится приемлемым, люди, получающие современную антиретровирусную терапию, даже безопасны для своих половых партнеров.
Есть и минусы: лекарства дорогие, а терапия пожизненная, причем действенность ее сильно зависит от того, насколько четко пациент соблюдает график приема. (Есть люди — их очень немного, — у которых после прекращения терапии инфекция десятилетиями не развивается из-за особенностей их иммунной системы, — так называемые элитные контроллеры, или нонпрогрессоры, — но это отдельная история.) В России лечение ВИЧ-инфицированных финансируется государством и субъектами федераций, антиретровирусные препараты входят в список жизненно важных, инфицированные получают их бесплатно. Однако из-за финансовых и бюрократических сложностей получают не все, кому они нужны. Например, как стало известно в конце марта 2019 года, пять тендеров на закупку антиретровирусных препаратов, объявленных Минздравом России, не состоялись из-за того, что начальная максимальная цена на поставку препаратов оказалась значительно ниже предельных отпускных цен. Это были ингибиторы обратной транскриптазы, в том числе ламивудин, который входит в большинство применяемых в России протоколов лечения ВИЧ. Из-за этого пациенты могут не получить препараты вовремя, а прерывать лечение опасно. Как-то этот вопрос решается, но представьте, каково следить за этими торгами пациентам.
Если это кого-то утешит (хотя утешение в эпоху глобализации так себе), во многих странах третьего мира ситуация с ВИЧ-терапией существенно хуже, чем у нас, и ни одна страна пока не может заявить, что полностью контролирует болезнь. Специалисты оценили с долей скепсиса даже недавнее обещание Дональда Трампа в ближайшие 10 лет покончить с ВИЧ на территории США. Амбициозную цель «90-90-90» поставила ЮНЭЙДС — организация, которая координирует международные меры противодействия СПИДу: к 2020 году 90% всех людей, живущих с ВИЧ, должны знать о своем статусе; 90% всех людей с диагнозом должны стабильно получать антиретровирусную терапию, и у 90% получающих ее вирус должен быть подавлен. Пока что предполагается, что на Земле около 36,7 млн людей живут с ВИЧ и около 70% узнали свой диагноз, антиретровирусная терапия доступна примерно половине, и только у 44% тех, кто лечится, вирус не определяется при анализах. Российское здравоохранение обещает предоставить терапию 75% пациентов с ВИЧ уже в 2019 году.
Есть ли альтернатива пожизненной антиретровирусной терапии? Неужели «медленный» вирус нельзя удалить из организма?
История первого излечения от ВИЧ-инфекции началась в 90-х годах. Врачи редко используют слова вроде «полное излечение», предпочитая говорить о «ремиссии» или «исчезновении вирусной нагрузки». Но в данном случае, поскольку пациент жив до сих пор, а должен был умереть еще в нулевые, слово «излечение» уместно.
 |
|
На скетче изображен Тимоти Рэй Браун.
Художник – Петр Перевезенцев
|
Американцу 1966 года рождения поставили диагноз «ВИЧ-инфекция» в 1995 году, во время его учебы в Берлине, поэтому его долгое время называли «берлинским пациентом». (Сейчас Тимоти Рэй Браун, проживающий в Калифорнии, отказался от анонимности и даже основал фонд своего имени для борьбы с ВИЧ/СПИДом.) К 2006 году у него развилась лейкемия, и в 2007 году ему сделали пересадку костного мозга в Берлинском университетском медицинском комплексе Шарите под руководством гематолога Геро Гюттера. Лейкемия, или лейкоз, — злокачественное заболевание клеток кроветворной системы, а кроветворные клетки находятся в костном мозгу, поэтому трансплантация здоровой ткани может помочь.
Интересно здесь и то, что трансплантанты были взяты от донора с мутацией в гене белка CCR5, того самого, с которым взаимодействует ВИЧ, чтобы проникнуть в клетку. Донора с такой мутацией выбрали сознательно — идея была в том, чтобы избавить человека и от лейкоза, и от ВИЧ.
В последние полгода о рецепторе CCR5 узнали даже далекие от биологии и медицины люди. Именно такой мутацией снабдил Хэ Цзянькуй двух генно-модифицированных китайских девочек (см. «Химию и жизнь», 2019, 4). Мутация Δ32 (удаление, или делеция 32 нуклеотидов) в гене CCR5 ведет к продукции мутантного, нефункционального белка, с которым вирус не может связаться, таким образом, она действительно защищает от ВИЧ-инфекции. (Но — внимание! — только от R5-тропных вариантов ВИЧ! Вариантам R5X4-тропным, распознающим другой корецептор, эта мутация не помеха.) В Европе, особенно Северной, мутация CCR5-Δ32 встречается намного чаще, чем в Африке или Азии, эту «несправедливость природы» и хотел исправить доктор Хэ.
Важно понимать, что означает «намного чаще». Частота мутантного аллеля (варианта гена, содержащего эту мутацию) у европейцев в среднем около 10%; в одном из исследований, в котором участвовали более 1,3 млн потенциальных доноров костного мозга из 87 стран мира, приводятся такие цифры: максимум — 16,4% в Норвегии, минимум — 0% в Эфиопии. И кстати, частота аллеля — это не то же, что частота встречаемости людей с мутацией. Все гены у человека представлены двумя копиями, поэтому у большинства носителей лишь один аллель мутантный, а другой – обычный. Такие люди (генетики называют их гетерозиготными) не полностью защищены даже от R5-тропных вариантов, хотя болезнь у них прогрессирует медленнее и на терапию они отвечают лучше. Людей, у которых обе копии мутантные (гомозиготных), считаные проценты: на Фарерских островах их целых 2,3%, для Европы обычно приводят среднее значение около 1%. В том же исследовании среди 7069 россиян нашлось 1,4% гомозиготных по этой мутации и 18,8% гетерозиготных. Тем не менее испорченный телефон СМИ превратил скучное «более процента россиян невосприимчивы к одному из вариантов ВИЧ» в удалое «русские устойчивы к СПИДу» — было бы это правдой, не знали б мы проблем с антиретровирусной терапией…
Кажется странным, что мутация, которая портит белок, могла получить такое относительно широкое распространение. Но есть версия, согласно которой CCR5-Δ32 в свое время снижала смертность от чумы, благодаря чему и закрепилась в европейской популяции. Имеются также данные в пользу того, что мутантный рецептор CCR5 может снизить реакцию «трансплантат против хозяина».
Однако у Тимоти Брауна реакция была тяжелейшая. Перед трансплантацией он прошел так называемое кондиционирование — уничтожение его собственных кроветворных клеток, пораженных раком; для этого ему назначали токсичные препараты и подвергали облучению. И все же из-за рецидива лейкемии ему потребовалась повторная трансплантация. Он получал сильные иммунодепрессанты, перенес искусственную кому и был на грани смерти. Но в итоге он победил и лейкемию, и ВИЧ — вирусные ДНК и РНК в его организме больше не находят, и антивирусные препараты он не принимает. (Хотя принимает профилактические препараты против вариантов вируса, которые используют другой корецептор, CXCR4, — от них он, естественно, не защищен. Если «берлинский пациент» был инфицирован обеими формами вируса и второй все еще скрывается в организме, то в отсутствие конкуренции со стороны «родственника» он может начать размножаться.)
«Я человек, у которого когда-то был ВИЧ. Я не мог полностью поверить, что вылечился, пока “New England Journal of Medicine” не опубликовал в феврале 2009 года отчет о моем случае. Уважаемый медицинский журнал говорил обо мне, убеждал в этом», — писал Браун в открытом письме, которое было зачитано на Конгрессе по стволовым клеткам пуповинной крови (Сан-Франциско, США) в июне 2012 года.
Путь «берлинского пациента» едва ли можно было назвать общедоступным. Из-за высокого риска опасных осложнений он подходил только людям, которым трансплантация костного мозга требуется в любом случае (то есть тем, у кого есть и ВИЧ-инфекция, и лейкемия или другое аналогичное по тяжести заболевание), а среди них — только тем, для которых удастся найти подходящего донора с мутацией и которые готовы пройти через страшные испытания. Сам Браун, рассказывая о лечении, употреблял слово «ад».
И все же над этим работают. Распространение спасительной мутации среди доноров изучают не просто так: чем обширнее будут базы данных, тем больше шанс на удачу для каждого пациента. Исследованиями возможностей трансплантации для лечения ВИЧ занимается, в частности, европейский научный консорциум. В базе данных IciStem около 22 тысяч доноров с мутацией Δ32 в гене CCR5. Консорциум отслеживает 38 ВИЧ-инфицированных человек, которым сделали пересадку костного мозга, в их числе шестеро получивших трансплантат от доноров без мутации.
Интересно, что у пяти из этих шестерых, по состоянию на ноябрь 2018 года, ВИЧ тоже не определяется. Предполагается, что вирус могла уничтожить мощная активация иммунной системы, которой сопровождалась трансплантация, — что, конечно, не отменяет защитного действия мутантных рецепторов. Но, может быть, именно крайне тяжелые подобные эффекты у Тимоти Брауна оказались для него спасительными?
Новый случай, о котором заговорили весной 2019 года, позволяет в этом усомниться. «Лондонский пациент», 36-й в списке IciStem, страдал от лимфомы Ходжкина, злокачественного заболевания лимфоидной ткани, и ему трансплантировали костный мозг от донора с мутацией CCR5 в мае 2016 года. Как и Браун, он получал иммунодепрессанты, но лечение было намного менее тяжелым — со времен берлинского пациента медицина продвинулась вперед. В сентябре 2017 года «лондонский пациент» прекратил принимать антиретровирусные препараты, и с тех пор, как минимум 18 месяцев, он в ремиссии.
«Я думаю, это немного меняет правила игры, — сказал доктор Равиндра Гупта, вирусолог из Лондонского университетского колледжа, первый автор статьи об этом успехе, опубликованной в Nature 5 марта 2019 года. — После “берлинского пациента” все верили, что нужно почти умереть, чтобы вылечиться от ВИЧ-инфекции, но теперь, возможно, это уже не так».
Ученые консорциума десятки раз анализировали кровь пациента. Один из тестов показал слабые признаки продолжающейся инфекции, но это могло быть результатом загрязнения в образце. Циркулирующего вируса не обнаружили и самые чувствительные тесты. Антитела к ВИЧ в крови присутствуют, но их уровни снижаются. «Я никогда не думал, что при моей жизни появится лечение», — сказал «лондонский пациент» в интервью газете «New York Times» 4 марта 2019 года.
Авторы статьи подчеркивают, что пока не могут дать гарантии полного излечения, однако общая картина внушает надежду. Еще один больной, под номером 19, — «пациент из Дюссельдорфа» — не принимает антивирусные препараты уже четыре месяца.
Из-за тяжелых побочных эффектов трансплантация костного мозга вряд ли будет массовым вариантом, даже если каждому из десятков миллионов инфицированных найдут подходящего донора. Однако есть альтернатива — ввести аналогичную мутацию в клетки самого пациента методами генного редактирования. Над подобным методом ВИЧ-терапии сейчас работает множество научных групп, хотя сообщений о таких успешных случаях, как «берлинский» и «лондонский пациенты», пока не было. Но кто знает, что ждет нас в будущем?
Эта статья доступна в печатном номере "Химии и жизни" (№ 6/2019) на с. 38 — 40.
