Экзосомы: пузырьки с ядом и лекарством
Экзосомы вызывают кальцификацию сосудов
Все видели рисунки и образовательные мультфильмы о том, как сердечно-сосудистая система транспортирует кровь по организму. Движение крови начинается в сердце: его левый желудочек сокращается и выталкивает кровь в артерии. В среднем объем крови, выброшенной одним ударом человеческого сердца в состоянии покоя, составляет 70 мл — это примерно половина объема теннисного мяча. В нашем теле около пяти литров крови, так что, если сердце бьется с частотой 72 удара в минуту, за эту минуту через него пройдет вся кровь. Когда мы бегаем или катаемся на лыжах, объем перекачиваемой крови увеличивается в восемь раз — до 40 литров в минуту. Самая крупная артерия, аорта, помогает сердцу в его нелегкой работе. Ее толстые эластичные стенки расширяются под давлением крови, поступающей из сердца, а затем вновь сжимаются и выталкивают кровь в сосуды.
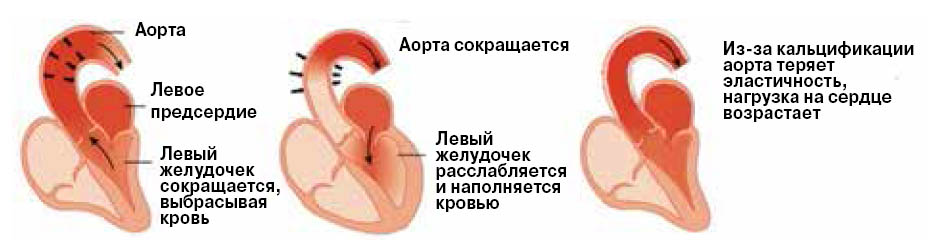
Старение, диабет второго типа, нарушения в работе почек и некоторые другие болезни вызывают структурные изменения в аорте. Она становится неэластичной и жесткой, кровь течет через нее уже не так легко, сердце должно прилагать для этого больше усилий (рис. 1). Проблема обостряется тем, что и к самому сердцу между ударами подается кровь — ведь наша главная мышца тоже нуждается в питании и кислороде, — но из-за уплотнения стенок аорты и других артерий кровоснабжение сердца уменьшается. Это, естественно, вызывает в его ткани дефицит кислорода, питательных веществ и вкупе с возросшей нагрузкой приводит к увеличению его объемов (гипертрофии). Человек начинает страдать от сердечной недостаточности.
|
|
1. Сокращаясь и расслабляясь, аорта помогает сердцу перекачивать кровь |
Известны две причины уплотнения сосудистых стенок. Первая — протеолитические ферменты, которые «переваривают» эластичные волокна, отвечающие за прочность и устойчивость стенок сосудов. Второй виновник — фосфат кальция, в норме — материал кости. Кристаллы этого вещества формируются прямо в аорте (рис. 2), внутри стенок сосудов, и при этом продуцируются белки, которые у здорового человека присутствуют только в костной ткани. В аорте эти белки играют двойственную роль. Некоторые из них, например матриксный Gla-белок (Matrix Gla Protein, или MGP), могут предотвратить кристаллизацию фосфата кальция, поэтому они называются ингибиторами минерализации. Но другие, такие, как фактор транскрипции Runx2, стимулируют его образование.
|
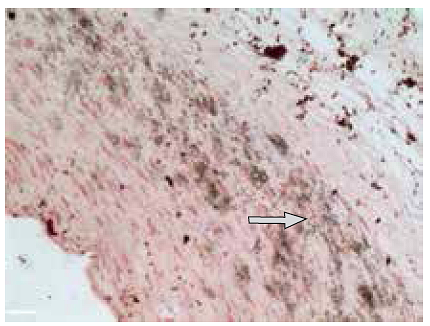
| 2. Обширные участки кальцификации в стенке аорты (показаны стрелкой) |
Баланс между ингибиторами и активаторами минерализации может быть легко нарушен. Именно это наблюдается при многих факторах риска: в пожилом возрасте, при курении, сахарном диабете второго типа и т. д. Например, у пациентов с хроническим заболеванием почек из организма плохо выводятся фосфаты, их уровень в крови растет, что, в свою очередь, стимулирует кальцификацию аорты. В результате у больных, которым назначают диализ, часто диагностируют кальцификацию сосудов. Половина таких пациентов умирает от болезней сердца.
Для решения этой проблемы важно было понять, какой компонент сосудистой стенки кальцинируется в первую очередь. Изучив литературу, мы обнаружили, что минерализация костей начинается в маленьких мембранных везикулах (пузырьках), которые секретируются костными клетками — хондроцитами. Эти везикулы впервые обнаружил в 1961 году доктор Кларк Андерсон. Он увидел их в электронный микроскоп, когда рассматривал костную ткань курицы, и назвал их «матричными везикулами».
Вскоре подобные везикулы нашли и внутри сосудистой стенки аорты. Работая с клеточными культурами, мы выяснили, что здесь эти везикулы выделяют клетки гладких мышц, образующие центральный слой аорты (Kapustin et al., 2015, «Circulation Research», 116, 8, 1312—1323, doi: 10.1161/CIRCRESAHA.115.306324). Именно эти везикулы делают стенки сосуда жесткими и неэластичными.
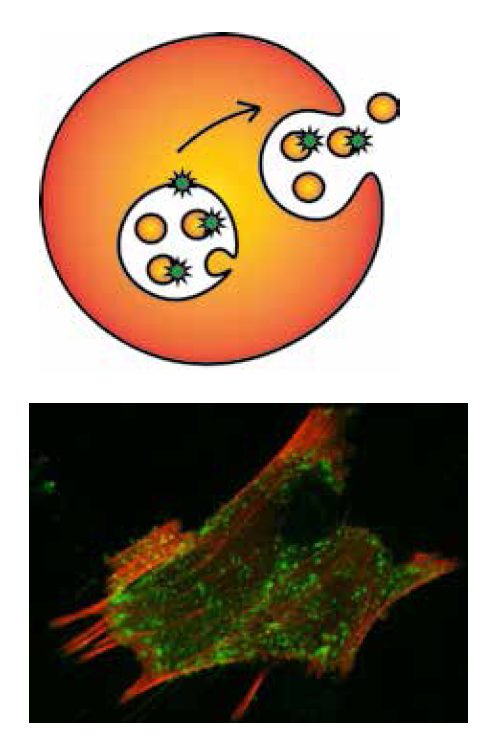
Обратившись к современным методам исследований в биохимии и клеточной биологии, с помощью мощных электронных микроскопов мы установили, что пузырьки размером около ста нанометров образуются в мультивезикулярных телах (рис. 3а, б). Они почкуются в полость внутри клетки, так что получаются пузырьки в пузырьке. В этих мультивезикулярных телах, или эндосомах, они отправляются к плазматической мембране и там высвобождаются из клеток гладких мышц, постепенно накапливаясь во внеклеточной ткани.
|
| 3. Экзосомы — мембранные пузырьки, которые клетка сначала отшнуровывает вовнутрь большого пузырька — мультивезикулярного тела, а потом выбрасывает во внешнюю среду. На микрофотографии — эндосомы внутри гладкомышечных клеток, помеченные зеленым флуоресцентным белком GFP |
Иначе говоря, это экзосомы — посылки в мембранной упаковке, которые клетка отправляет во внешний мир (подробнее см. «Химию и жизнь», 2013, 6).
Все больше данных свидетельствуют о том, что такие экзосомы производятся и высвобождаются преимущественно при наличии сердечно-сосудистых факторов риска, способствующих кальцификации, — например, при повышении уровня кальция или фосфатов в крови пациентов, у которых нарушена работа почек.
|
|
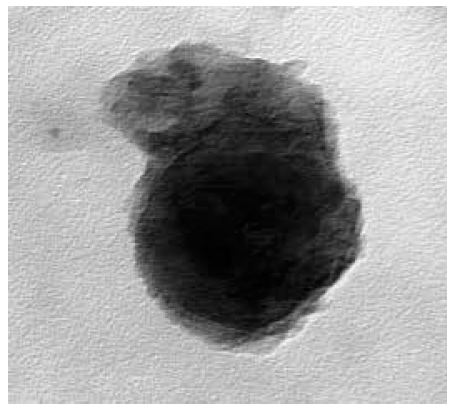
4. Экзосома с аморфным фосфатом кальция (темная область внутри) |
На рис. 4 можно увидеть самые первые кристаллы в экзосомах, которые образуются в аорте, — эти экзосомы мы получили из клеток гладких мышц аорты человека в эксперименте по их культивированию. Со временем они превращаются в крупные «камешки» (рис. 5), которые затем объединяются и формируют области кальцификации, показанные на рис. 2.
|
|
5. «Камешки» в стенке аорты человека |
Такие изменения фактически ответственны за смертность от сердечно-сосудистых заболеваний. Поэтому в будущих исследованиях мы планируем выяснить, почему высвобождаются экзосомы, какие факторы стимулируют и тормозят этот процесс и как можно регулировать заполнение экзосом именно теми белками, которые подавляют кальцификацию. Кроме того, сейчас можно достоверно обнаружить кальцификацию только с помощью рентгенологического исследования, поэтому необходимо разработать более простые и доступные клинические тесты для диагностики. Это помогло бы предотвратить кальцификацию сосудов в группах высокого риска, например у пациентов с хроническими заболеваниями почек.
Экзосомы защищают сердце
Если выложить в ряд один за другим все кровеносные сосуды в нашем теле — артерии, капилляры и вены, — их суммарная длина составит около 100 000 км, что примерно в 2,4 раза больше окружности Земли. Чтобы качать кровь через все эти сосуды, нужен по-настоящему мощный насос. Сердце первым из всех органов начинает работать в развивающемся эмбрионе и не останавливается вплоть до смерти человека. На протяжении нашей жизни оно делает около 3 миллиардов ударов. (Любопытно, что и у мышей за их короткую жизнь сердце сокращается столько же раз, как и у медведей, китов или у любого другого млекопитающего, — но это уже другая история).
К сожалению, с возрастом кровеносные сосуды постепенно повреждаются. Эти повреждения многократно усиливаются, если мы курим, не занимаемся спортом и не питаемся правильно. Артерии умеют восстанавливаться, отстраивая заново поврежденные участки, но с течением времени становятся все более узкими и слабыми, а в худшем случае артерия полностью закупоривается.
Коронарные артерии, снабжающие кровью сердце, называются так потому, что напоминают по форме корону. Когда они блокируются, участок ткани сердца больше не получает кровь — а значит, кислород и питательные вещества. Это явление называется ишемией. В течение нескольких секунд у сердца заканчивается энергия, и оно перестает нормально биться, происходит инфаркт. Для организма это чрезвычайная ситуация. Повреждение сердца посылает очень сильный болевой сигнал в мозг — этого, как правило, достаточно, чтобы заставить человека вызвать «скорую помощь». Человек должен попасть в больницу как можно раньше, чтобы врачи попытались раскупорить кровеносный сосуд и восстановить поток крови к сердцу. Если пациенту повезет, это удастся сделать и часть сердечной мышцы будет сохранена, но чаще всего орган повреждается непоправимо. В течение многих лет ученые пытаются найти способ защитить сердце от таких повреждений.
Важные открытия часто делаются тогда, когда эксперимент дает неожиданный результат и ученый оказывается достаточно умным, чтобы понять его причины. Американские ученые проводили эксперименты на собаках, чтобы понять, какие факторы усугубляют ущерб от сердечного приступа («Circulation», 1986, 74, 1124—1136). Они намеренно блокировали коронарные артерии у животных под наркозом в течение тридцати минут, а затем исследовали повреждения сердца. Исследователи пытались выяснить, могут ли несколько пятиминутных пауз в кровоснабжении сердца усугубить повреждения при последующем приступе. Интуитивно они ожидали положительного ответа, но получили неожиданный результат: небольшие остановки кровоснабжения примерно вполовину уменьшили степень повреждения сердца! Это явление получило название ишемического прекондиционирования: короткие периоды ишемии подготовили сердце к защите от последующего длительного приступа.
Ученые предположили, что ишемическое прекондиционирование можно использовать, чтобы защитить сердце пациента от серьезных повреждений. Правда, возникает небольшая проблема: как понять, что нужно обеспечить пациенту ишемическое прекондиционирование, если вы не знаете, когда у него будет сердечный приступ? И кто возьмется оперировать человека с целью устроить ему небольшой сердечный приступ, чтобы защитить его от большого, который может и не случиться? Парадоксальная ситуация: само по себе явление очень интересно, и ученые потратили годы на исследование его механизма, но возможности использовать его при лечении нет.
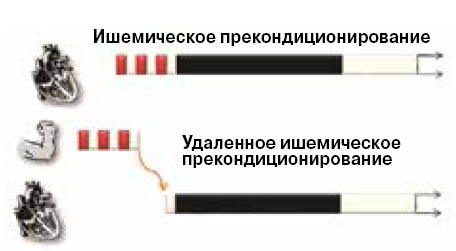
Наконец, в 2002 году у ученых возникла сумасшедшая идея: а что, если ишемическое прекондиционирование произойдет в другом органе, например в печени, или почке, или даже в руке? Ведь достаточно надуть манжету для измерения давления на руке до чуть более высоких, чем обычно, значений, чтобы полностью блокировать приток крови в руку, — и это уже ишемия! (Вообще, «ишемия» — это местное снижение кровоснабжения, от греческих слов ίσχω — задерживаю, останавливаю и άιμά — кровь. Так что ишемия, вопреки распространенному мнению, бывает не только в сердце.) И в самом деле, эксперименты показали, что нескольких коротких периодов ишемии в конечности достаточно, чтобы защитить сердце от последующего повреждения. Рука как будто посылает предупредительные сигналы к сердцу: «Эй! Осторожно! У меня ишемия, возможно, она направляется к тебе!» Это явление вполне логично было названо «удаленным ишемическим прекондиционированием» (рис. 6).
|
|
6. Предварительные кратковременные перебои в кровоснабжении сердца не усугубляют, а смягчают последствия инфаркта. Но еще удивительнее, что такой же эффект дает ишемия конечности. Причина же, очевидно, в экзосомах, которые рука посылает к сердцу |
Конечно, эти исследования пока находятся на стадии проверки гипотез. Мы до сих пор не знаем, насколько надежна защита, которую дает этот механизм.
Но если он будет работать, у нас появится простой способ предотвратить повреждения сердца у людей с высоким риском сердечного приступа. Во всяком случае, это гораздо проще, чем вскрывать им грудную клетку!
Пока что ученые во всем мире пытаются ответить на главный вопрос: «Как это работает?» Несколько лет назад наша команда предположила, что в этот процесс могут быть вовлечены экзосомы — маленькие гонцы, способные доставлять сообщения в организме, преодолевая значительные расстояния как раз с помощью кровеносной системы. Может быть, это они передавали сигналы от ишемизированной конечности к сердцу?
Мы измерили количество экзосом в крови до и после удаленного ишемического прекондиционирования и увидели, что после ишемии их гораздо больше! При этом, как выяснилось, эти экзосомы действительно могут отправить защитные сигналы к сердцу.
Научные исследования часто развиваются в неожиданных направлениях. Так и мы на следующем этапе исследований установили еще более удивительный факт: на самом деле миллиарды экзосом были в крови еще до того, как мы провели прекондиционирование, и эти экзосомы тоже были защитными! Мы очистили с помощью ультрацентрифугирования экзосомы из крови крысы, чтобы проверить их действие на сердце (Vicencio et al., «Journal of American Col- lege of Cardiology», 2015, 65, 15, 1525— 1536, doi: 10.1016/j.jacc.2015.02.026). Для этого мы использовали две экспериментальные модели. Одна — in vitro: клетки сердца, кардиомиоциты, поместили в специальный инкубатор с пониженным содержанием кислорода; таким образом моделировался момент ишемии (гипоксии). Затем содержание кислорода резко повышали до 21%, так мы вызывали эффект резкого восстановления кровоснабжения (реоксигенации). Эта последовательность событий имитирует развитие инфаркта.)
Обработка клеток экзосомами перед циклом «гипоксия-реоксигенация» значительно повышала устойчивость клеток к стрессам и увеличивала их жизнеспособность.
Вторая модель — in vivo, то есть в целостном организме: коронарную артерию сердца крысы под наркозом зажимали с помощью лигатуры на 30 минут, а потом перевязку удаляли, восстанавливая кровоснабжение. Именно так зачастую протекает инфаркт в сердце человека, когда гипоксия и реоксигенация последовательно наносят повреждение ткани сердца. Инъекция экзосом перед зажиманием сосуда также увеличивала жизнеспособность клеток в зоне инфаркта.
Чтобы понять, каким образом экзосомы это делают, мы добавляли к клеткам химические ингибиторы различных сигнальных систем и смотрели, сохраняется ли защитный эффект. Как оказалось, экзосомы содержат белок теплового шока HSP70, который связывается с рецептором клетки TLR4. Это активирует сигнальные каскады, которые, в свою очередь, защищают «энергетические станции» клетки, митохондрии, от разрушения в условиях гипоксии-реоксигенации и таким образом спасают клетку от гибели.
Исследования экзосом — захватывающая и малоизученная область медицины. Нам еще очень многое предстоит узнать о том, что эти наночастицы делают в нашей крови. Но мы надеемся, что в один прекрасный день сможем взять часть экзосом, улучшить их воздействие с помощью суперзащитных молекул и ввести обратно в кровь пациенту, чтобы защитить его от сердечного приступа. Или, возможно, удастся сделать пилюли с экзосомами? Представьте себе рекомендацию врача: «Просто принимайте один миллиард этих нанотаблеток каждый день!»
Профессор Кэтрин Шанахан руководит научной группой в Лондонском королевском колледже, изучает проблемы сосудов при различных заболеваниях и старении. Александр Капустин — постдок в группе профессора Шанахан, координатор российско-британских семинаров «Researcher Links» Британского Совета. Тематика его исследований — выяснение роли экзосом в ранозаживлении сосудов. Шон Дэвидсон — научный сотрудник Лондонского университетского колледжа, его основные научные интересы — разработка новых методов защиты сердца от инфарктов.
