Умные ножницы для ДНК
 Бактерии и археи не имеют такой иммунной системы, как мы с вами, — это в принципе невозможно, у нас за иммунитет отвечает множество клеток, а бактерия существо одноклеточное. Однако бактерии не беззащитны против вирусов-бактериофагов и других патогенов. Система элементов геномной последовательности, называемая CRISPR, и ассоциированные с ней белки Cas помогают им распознавать и уничтожать чужеродный генетический материал.
Бактерии и археи не имеют такой иммунной системы, как мы с вами, — это в принципе невозможно, у нас за иммунитет отвечает множество клеток, а бактерия существо одноклеточное. Однако бактерии не беззащитны против вирусов-бактериофагов и других патогенов. Система элементов геномной последовательности, называемая CRISPR, и ассоциированные с ней белки Cas помогают им распознавать и уничтожать чужеродный генетический материал.
В 1987 году в геноме кишечной палочки Escherichia coli был обнаружен загадочный участок, состоящий из многочисленных повторов (A.Nakata et al., «Journal of Bacteriology», 1989, 171, 3553—3556). Функция этого участка, названного CRISPR-локусом (произносится «криспер»), долгое время оставалась загадочной. Но в 2005 году сразу три группы сообщили, что разделяющие эти повторы промежуточные последовательности зачастую бывают идентичны последовательностям, найденным в геномах бактериофагов и в плазмидах. (Плазмиды — кольцевые молекулы ДНК, путе- шествующие из одной бактериальной клетки в другую. С их помощью бактерии обмениваются полезными генами, например устойчивости к антибиотикам, но, с другой стороны, некоторые плазмиды обладают чертами «комплекса эгоистичных генов» — используют бактериальную клетку как копирующее устройство, фактически паразитируя на ней.)
Эти данные позволили предположить, что локус CRISPR — часть ранее не известного механизма, который предназначен для защиты бактерий и архей от инфекций. Дальнейшая судьба защитной системы CRISPR/Cas еще интереснее — в 2012—2013 годы на ее основе были изобретены высокоточные инструменты для редактирования генов, а также для управления их активностью. И, судя по всему, это только начало ее карьеры в современной биотехнологии.
Коллекция трофеев
Название локуса CRISPR — фактически его словесный портрет: «скопление разделенных регулярными промежутками коротких симметричных повторов» (clustered regularly interspaced short palindromic repeats). Описание абсолютно верное: короткие повторы чередуются с неповторяющимися последовательностями, как в детском стишке Даниила Хармса: «Чиж-судомойка, чиж-поломойка, чиж-огородник, чиж- водовоз...» — только вместо «чижа» палиндром, одинаково читающийся с обоих концов. (О палиндромах в поэзии и в ДНК см. статью Б.Я.Бейнфеста в этом же номере). В каждом конкретном локусе все повторы практически одинаковы и имеют длину от 24 до 48 пар нуклеотидов. Промежутки также примерно одинаковы по длине (21—72 п. н.), но весьма вариабельны по последовательности.
Так вот, эти промежуточные последовательности, или спейсеры, часто происходят из плазмид и фагов. Бактерии, выжившие после атаки фага, в результате так называемой адаптации пополняют свой CRISPR за счет спейсеров, идентичных небольшим «трофейным» участкам ДНК фага (R.Barrangou et al. & P.Horvath, «Science», 2007, 315, 1709—1712). А значит, спейсерные последовательности массива CRISPR — это память бактерии-хозяина о вирусных инфекциях и встречах с инородным генетическим материалом.
|
|
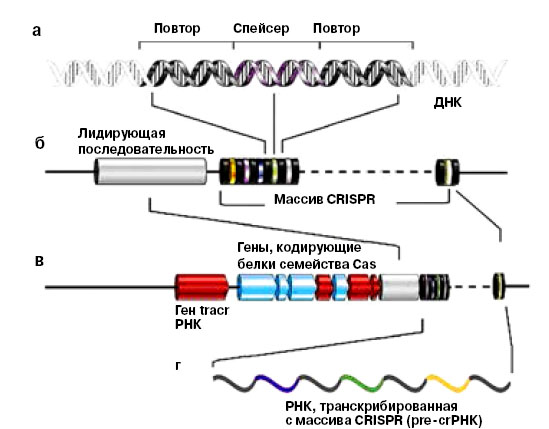
1. Структура локуса CRISPR): а — строение участка CRISPR; б — массив CRISPR и лидерная последовательность; в — те же и «соседи» — гены, кодирующие tracrРНК, и гены белков семейства Cas; в — молекула РНК, возникшая при транскрипции массива CRISPR; как и в самом CRISPR, в ней чередуются повторы и разнообразные участки, комплементарные участкам геномов, нападавших на бактерию плазмид и фагов (по: «Molecular Сell», 2010, 37, 7—19) |
К локусу CRISPR примыкает лидерная последовательность (длиной до 550 п. н.), а также CRISPR-ассоциированные гены (CAS), кодирующие белки семейства Cas. Лидерная последовательность играет роль промотора — стартовой площадки, с которой начинается транскрипция массива CRISPR, то есть «переписывание» последовательности на РНК (рис. 1). Кроме того, возможно, что лидерная последовательность узнает белки, участвующие во встраивании новых спейсеров: как новые участки ДНК от нападавших микроорганизмов, так и новые повторы обычно встраиваются на границе между ней и CRISPR (рис. 2).
|
|
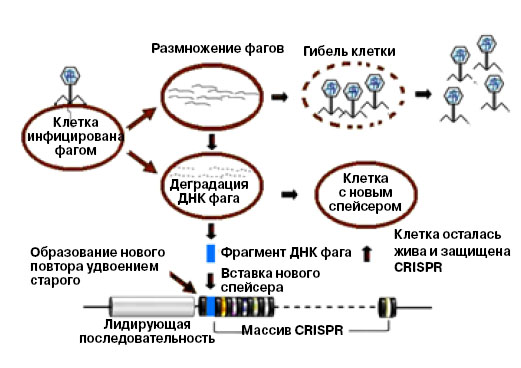
2. Пополнение коллекции фрагментов чужеродной ДНК в системе CRISPR-Cas. После расщепления ДНК фага или плазмиды «трофейный» фрагмент вставляется в локус CRISPR в качестве спейсера. Затем он будет использован как шаблон для создания малых молекул crРНК. С помощью комплексов crРНК и белка Cas9 бактерия защищается от инфекций. |
Длинная молекула РНК, которая образуется после транскрипции CRISPR, разрезается на фрагменты. Они называются CRISPR РНК (crРНК), причем каждый содержит спейсер и часть повтора. В процессе нарезки участвует небольшая РНК, комплементарная повторам, — tracrРНК: она служит «наводчицей» для белка Cas9, к которому подсоединяется фермент РНКаза III, нарезающий длинную молекулу РНК. Исполнив свою роль, РНКаза III уходит. Остается комплекс двух молекул crРНК и tracrРНК с белком Cas9. Этот белок — нуклеаза, то есть фермент, разрезающий ДНК. Сам по себе Cas9 неактивен, но при связывании с tracrРНК его трехмерная структура изменяется, и он приобретает способность взаимодействовать с ДНК-мишенью — защелкивается на ее двух нитях, превращаясь в нечто подобное замку застежки-«молнии».
А затем комплекс crРНК/tracrРНК-Cas9 начинает расправу с врагом: спейсерные участки crРНК находят комплементарные им участки вражеских нуклеиновых кислот и приносят к ним активированные Cas-белки, те вызывают их расщепление и последующую деградацию. (Этот механизм отчасти напоминает РНК-интерференцию эукариот, см. статью «Вид с вершины» в этом же номере.) Таким образом, crРНК выполняет роль проводника, направляющего нуклеазу к цели, за что она и получила свое другое название: «РНК-гид» (рис. 3).
|
|
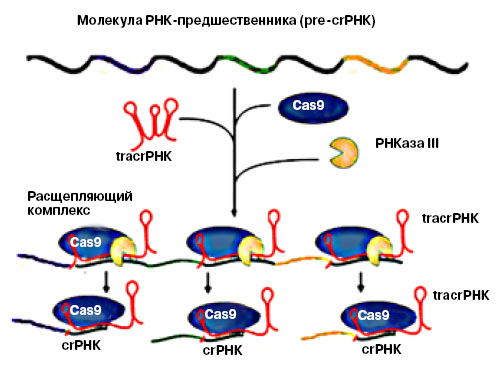
3. Так образуются комплексы crРНК/tracrРНК-Cas9—оружие иммунной системы прокариот (по: «Nature», 2011, 471, 7340, 602—607). Фермент РНКаза III и белок Cas9 распознают tracrРНК, комплементарную последовательностям повторов в цельной молекуле РНК-предшественника (pre-cr РНК). Расщепление, по всей видимости, происходит в середине повтора. Образуются crРНК, каждая из 42-нуклеотидов: 22 «хвостовых» — остаток повтора, остальные 20 — уникальный спейсерный фрагмент, который помогает белку Cas9 искать инородную ДНК |
Чтобы белки Cas узнали и затем расщепили опознанную РНК-гидом последовательность ДНК, непосредственно после сайта-мишени должна находиться короткая (от трех до девяти нуклеотидов) последовательность, называемая PAM — protospacer adjacent motif. Таким образом, атакуются только те участки вражеской ДНК, рядом с которыми находятся эти короткие последовательности. У разных видов бактерий РАМ различаются. Если участок ДНК комплементарен crРНК, но рядом с ним нет РАМ, то комплекс crРНК/tracrРНК-Cas9 его не распознает. У этой особенности есть биологическое объяснение, пока экспериментально не подтвержденное. Дело в том, что в локусе CRISPR наряду со спейсерами, комплементарны- ми инородной ДНК, встречаются и спейсеры, нацеленные на собственную ДНК бактерии. И таких спейсеров-«самоубийц» немало — порядка 20%. Гены эти, однако, не разрушаются, возможно, из-за отсутствия рядом с ними PAM («PLoS Genetics», 2013, 9(9), e1003742, doi: 10.1371/journal.pgen.1003742). Роль спейсеров, комплементарных «своей» ДНК, предстоит еще выяснить. Возможно, бактерия с их помощью регулирует не расщепление генов, а их транскрипцию, используя другие белки.
Интересно, что если заразить клетки неизвестным им фагом, то лишь три процента выживших бактерий удлиняют свою CRISPR-кассету на один спейсер, соответствующий новому фагу. Если же клетки заразить фагом, ДНК которого хотя бы отчасти сходна с каким-либо спейсером в CRISPR-кассете, то адаптация идет гораздо активнее. От 50% до 90% популяции пополняет свои CRISPR участками генома этого фага, и выживаемость возрастает в десятки раз. Этот процесс был назван праймингом («Nature Communications», 2012, 3, 945, doi:10.1038/ ncomms1937; не столь уж частый случай, когда в примечаниях к статье можно увидеть московские институты и российские гранты: один из ведущих авторов этой и предыдущей публикации — доктор биологических наук К.В.Северинов). Возможная причина в том, что после опознания белком Cas9 стартовой площадки — PAM — с ДНК-мишенью сначала связывается лишь небольшой участок спейсера (6—12 нуклеотидов), называемый затравкой, и лишь затем остальная часть спейсера. Если на участке затравки комплементарность строго соблюдается, то на остальной части спейсера возможны отклонения, иногда до 3—5 п. н. Бактерии эта неточность на пользу, благодаря ей она может успешно опознать фаги-мутанты и быстро настроиться на поражение новых целей. А вот ученым предстоит разработать методы, повышающие точность распознавания, — в работе «генного скальпеля», о котором пойдет речь дальше, всякую приблизительность необходимо исключить. Возможным выходом может стать использование crРНК с усеченной спейсерной частью («Nature Biotechnology», 2014, doi:10.1038/nbt.2808).
Напоследок отметим, что у некоторых фагов найдены гены, способные ингибировать систему CRISPR-Cas, и они также весьма интересны в плане практического применения.
Для чего и как используют технологии CRISPR-Cas9
Использование адаптирующейся иммунной системы бактерий началось еще в 2007 году, когда фирма «Дюпон» создала устойчивые к вирусной инфекции бактериальные штаммы для производства продуктов питания (в этих опытах бактерий вакцинировали разрушенными вирусами). Однако подлинный бум начался в конце 2012 года, после того, как Мартин Джинек сумел объединить tracrРНК и crРНК в одну цельную молекулу РНК — теперь ее называют РНК гидом, или sgРНК, от англ. single-guide RNA — и изобрел вектор для клонирования этой РНК (M.Jinek, K.Chylinski, I.Fonfara et al. «Science», 2012, 337, 816—821, doi: 10.1126/science.1225829).
Оказалось, что такая синтетическая sgРНК образует комплекс с белком Cas9 ничуть не хуже, чем tracrРНК и crРНК, а затем находит комплементарные ДНК и правильно ориентирует Cas9, чтобы создавать в них двухцепочечные разрывы (рис. 4). Причем может сделать это именно в том участке, в каком пожелает исследователь, — достаточно включить в sgРНК фрагмент, комплементарный этому участку. Конечно, выбрать надо такую последовательность, которая встречается только в нужном вам месте и не повторяется там, где разрезы не нужны. Иначе экспериментатор окажется в положении неумелого пользователя, который скомандовал текстовому редактору найти и удалить из рассказа имя «Оля» и с удивлением увидел, что пострадали также «Коля», «поля» и «тополя». После того, как разрез в нужном месте сделан, клетка сама стремится его ликвидировать с помощью процесса, называемого репарацией.
|
|
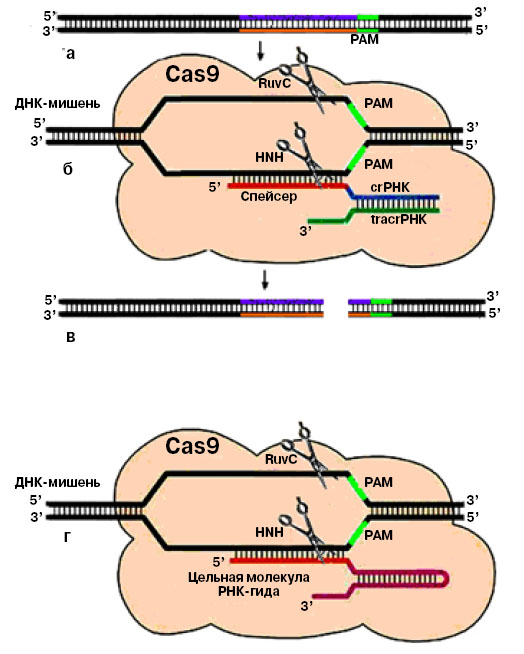
4. Принцип работы Cas9 в природе (с участием crРНК и tracrРНК) и в составе искусственной конструкции, где одна молекула sgРНК заменяет две.Вверху: двухцепочечная ДНК-мишень подвергается точному разрезанию: Cas9 распознает мишень с помощью crРНК, а та удерживается в молекуле Cas9 благодаря посредничеству tracrРНК. Места разрезов обозначены ножницами. RuvC и HNH — домены (части) Cas9; оба они обладают нуклеазной активностью, каждый разрезает одну из двух нитей ДНК. Внизу — тот же процесс с участием цельной молекулы sgРНК, созданной усилиями ученых; она взаимодействует и с Cas9, и с ДНК-мишенью |
Как внедрить в клетку высокоточный генный скальпель, состоящий из sgРНК и Cas9? Для этого можно использовать так называемый all-in-one CRISPR-Cas9 cloning vector — кольцевую молекулу ДНК, которая кодирует sgРНК и матричную РНК белка Cas9. Такие векторы, с возможностью вставить в нужное место участок, комплементарный вашей мишени, уже предлагают биотехнологические фирмы. Естественно, кроме кодирующих последовательностей, там будут и управляющие, которые подскажут клетке, откуда надо считывать РНК.
Купив такой вектор и вставив в него «свою» последовательность, исследователь нарабатывает его в необходимом количестве методом молекулярного клонирования. Вектор внедряют в клетки специального лабораторного штамма кишечной палочки, затем растят бактерий на питательной среде, причем они многократно копируют вектор (это и называют молекулярным клонированием). Копируют, но «не читают», sgРНК и Cas9 в бактериальных клетках не синтезируются — командные сигналы в векторе адресованы другому организму. Потом вектор выделяют из бактерий и трансформируют им клетки, геном которых мы хотим отредактировать. Вот в них-то и начнут синтезироваться РНК-гид и Cas9.
Это изобретение генных инженеров еще в начале 2013 года доказало свою эффективность на человеческих клетках в культуре. После инфицирования клетки CRISPR-Cas9-вектором в ней действительно появился комплекс Cas9-sgРНК, который затем проникал в ядро и находил соответствующие последовательности ДНК (eLife; 2:e00471, doi: 10.7554/eLife.00471, «Nature Biotechnology», 2013, 31, 230—232).
В течение 2013 года технологии CRISPR были опробованы почти на всех модельных видах, используемых в экспериментах. На бактериях комплексы Cas9-sgРНК проявили себя как высокоизбирательный «умный антибиотик» — с их помощью из смешанной культуры бактерий удаляли отдельные виды и штаммы; «скальпель» рассекал специфичные для них последовательности, не трогая остальных. Они показали себя простым и мощным инструментом генной инженерии в опытах с дрожжами, плодовыми мушками, рыбками данио. Появились на свет мыши, обезьяны, свиньи с прицельно выполненными мутациями. Инъекции матричной РНК Cas9 и sgРНК в клетки зародыша позволяют быстро, всего за одну стадию, получить свиней с модифицированным геномом и таким образом создавать модели для изучения генетических заболеваний человека и животных и тестировать на них новые методики лечения. Этот же метод можно применять и для улучшения пород сельскохозяйственных животных и сортов растений.
Программируемые РНК-гидом нуклеазы были использованы для целенаправленного редактирования генома в клетках человека («Nature Biotechnology», 2013, 31, 230—232). Понятно, что такая возможность внушает опасения. Но если говорить о реальных, а не фантастических применениях, подобное редактирование — прежде всего мощный инструмент исследования. Например, выключая с помощью CRISPR-Cas9 отдельные гены, можно идентифицировать те, что отвечают за выживание клеток при раке («Science», 2014, 343, 6166, 84—87). Более того: обнаружив в отдельных клетках организма мутации, которые ведут к развитию рака, можно будет, используя аналогичные методы, убрать их («Genome Medicine», 2014, 6, 5). За короткие сроки была синтезирована огромная библиотека РНК-гидов с различными последовательностями — 73 000 различных sgРНК («Science», 2014, 343, 6166, 80—84). С ее помощью можно направлять Cas9 на 80—90% всех последовательностей генома человека.
Резонный вопрос: неужели до 2013 года у молекулярных генетиков не было инструментов для разрезания ДНК в нужной точке? Были, но значительно менее удобные. Например, искусственные ферменты, получаемые путем слияния ДНК- разрезающего домена нуклеазы с ДНК-связывающим доменом другого белка. Для каждой ДНК-мишени приходилось кропотливо конструировать новый фермент. По сравнению с этими конструкциями система CRISPR, где в качестве нуклеазы используется один и тот же Cas9, а менять приходится лишь sgРНК, оказалась намного проще и дешевле. То, на что уходили месяцы и годы труда, удается сделать за неделю.
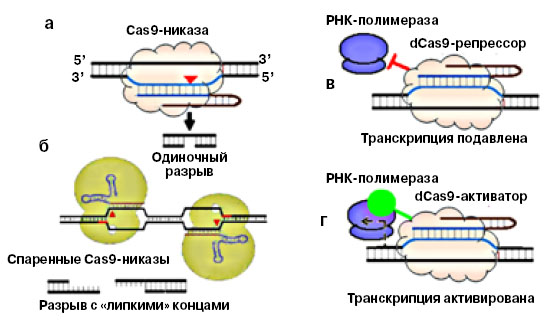
Напоследок, для тех, кто еще не устал, — несколько слов о других применениях CRISPR-Cas9 (рис. 5). Наряду с обычным «природным» Cas9, который делает двухцепочечные разрывы в ДНК, ученые используют его измененные формы. Первой стоит упомянуть Cas9-никазу — белок, у которого активна только одна из его нуклеаз, а другая инактивирована. Такой фермент делает разрыв только в одной из двух цепей ДНК. Используя парочку таких никаз с разными sgРНК, можно значительно повысить точность генного скальпеля, а кроме того, вырезать большие участки ДНК (Cell, 2013, 154, 1380—1389).
|
|
5. Модификации белка Cas9: а — Cas9, у которого активна только одна из его нуклеаз, а другая инактивирована, разрезает только одну нить ДНК, называется Cas9-никазой; б — две Cas9-никазы с разными sgРНК разрезают ДНК с образованием «липких» — одноцепочечных концов; в — мутантный белок dCas9, у которого инактивированы обе нуклеазы, можно использовать для выключения гена, регуляторному участку которого комплементарна sgРНК; г — подобным же образом можно избирательно активировать синтез определенных генов |
У мутантного белка dCas9 инактивированы обе нуклеазы. Он находит ДНК-мишень и связывается с ней, но не способен ее разрезать. Казалось бы, какая польза от тупых ножниц? Однако из них можно сделать хороший зажим или прищепку. Белок dCas9 применяют для инактивации генов на стадии транскрипции — он блокирует продвижение РНК-полимеразы, того самого фермента, который синтезирует РНК на матрице ДНК. Этот способ называется CRISPR- интерференцией, или CRISPRi («Cell», 2013, 152, 1173—1183). Аналогичным способом можно не полностью выключать транскрипцию, а избирательно менять ее активность. Для этого к dCas9 добавляют домен белка — фактора транскрипции, который увеличивает или подавляет активность генов, а затем снабжают его sgРНК, которая доставит эту конструкцию на регуляторный участок — промотор нужного гена.
И еще один интересный инструмент — зажим с фонариком. Прикрепив к белку dCas9 зеленый флуоресцентный белок EGFP, можно пометить им определенный участок в хромосоме живой клетки и наблюдать под микроскопом за его судьбой в течение клеточного цикла либо визуально определять длину теломер («Cell», 2013, 155, 1479—1491).
Что впереди?
Крошечная молекулярная машина, защищающая бактерии от вирусов, а также изобретательность и находчивость ученых помогли совершить революцию в генной инженерии, существенно упростив и удешевив технику редактирования геномной ДНК. В перспективе эта технология может значительно ускорить темпы развития экспериментальной биологии и генной терапии, подарит медицине «умные антибиотики»; поможет в проектировании и создании генно-модифицированных сельскохозяйственных животных и растений, а также промышленных микроорганизмов.
Но чтобы сделать технологию безопасной, надо исключить все возможные побочные эффекты — добиться, чтобы комплекс Cas9-sgРНК направлялся именно туда, куда мы хотим его направить, и делал именно то, что от него требуется. Для этого его нужно всесторонне проверить в самых разных условиях и детально прояснить механику его действий. Думается, что возможные применения CRISPR-Cas9-технологии не исчерпаны теми, о которых мы только что рассказали.
